
类器官(Organoids)来源于机体自身组织或干细胞,是通过体外3D培养形成的具有原始组织及器官的3D结构模型。近年来,类器官研究在国自然中标项目中呈现明显的增长趋势,那么关于类器官有什么课题设计思路呢?今天我们一起来探讨一下。
今天我们将分享一篇发表于中科院1区期刊Advanced Science,影响因子为14.3的文献,希望能给大家带来不一样的灵感。
一、课题挂靠与SCI信息

【文章题目】:WT1突变的肾脏类器官模型揭示了足细胞发育中关键调控路径
【发表期刊】:Advanced Science
【影响因子】:14.3/中科院1区
【课题挂靠】:2021YFC2501302/国家重点研发计划;BK20210150/江苏省自然科学基金;LQ24H050001/浙江省自然科学基金;2023TQ0293/中国博士后科学基金;32141004/国家自然科学基金
二、研究背景
①足细胞(podocyte)是肾脏中的一个特殊细胞类型,负责维持肾小球的过滤功能;
②在肾脏发育过程中,肾母细胞瘤抑制基因(WT1)的表达随着后肾间充质和足细胞祖细胞的发育而增加,最终局限于成熟足细胞;
③WT1突变导致各种足细胞表现,并伴有肾小球基底膜缺陷;
④肾类器官是探索患者基因突变致病机制的一种完善的疾病模型。
三、技术路线
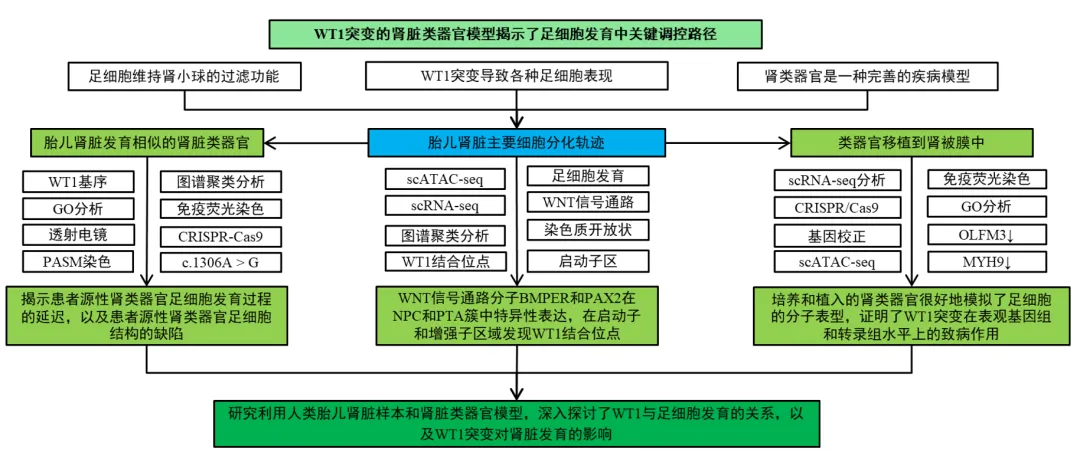
四、研究结果
1.确定胎儿肾脏主要细胞分化轨迹中人类足细胞发育的WT1相关表观基因组景观
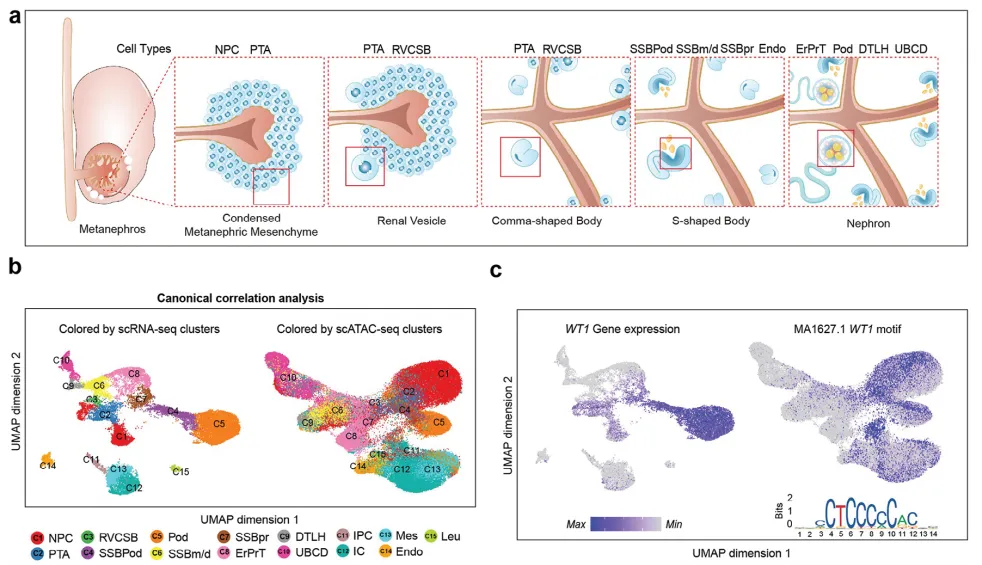
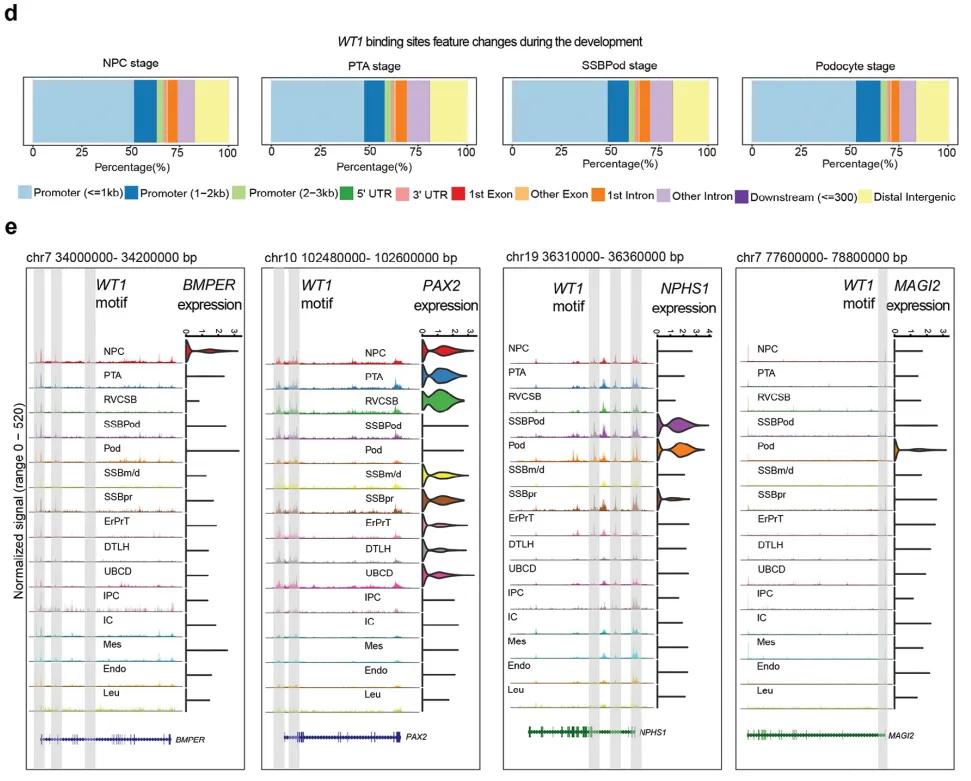
首先,在图1a~c中,他们获取了胎儿肾脏发育过程中不同细胞群的染色质动力学数据,接着通过scATAC-seq、scRNA-seq数据,进行相关图谱聚类分析,形成胎儿时期肾脏发育的基础模型,并提示WT1在胎儿肾脏发育过程中可能有重要作用。图1d显示,在足细胞发育过程中,WT1结合位点的全局分布没有改变,主要位于基因启动子和假定的远端增强子。进一步研究发现,WT1在NPC、PTA、SSBPod和足细胞簇中的染色质开放状态与基因表达具有较高一致性,表明WT1在足细胞的发育过程中起到了重要的作用。最后发现,WNT信号通路分子BMPER和PAX2在NPC和PTA簇中特异性表达,并且在这两个基因的启动子和增强子区域也发现了WT1的结合位点。
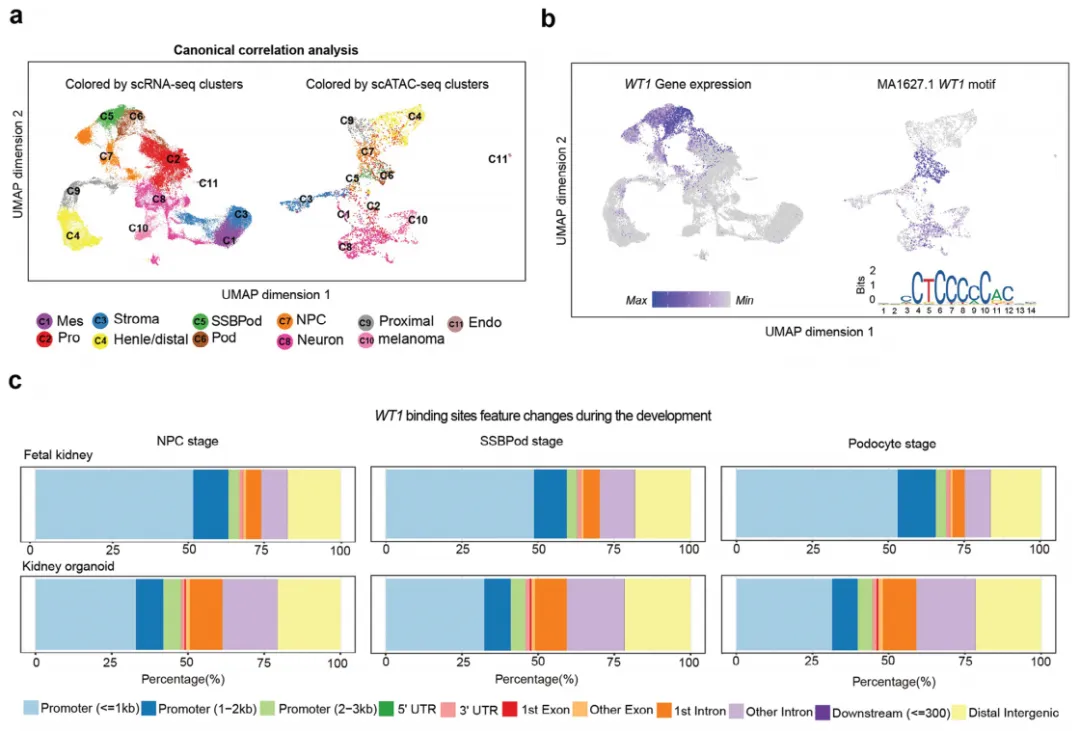
2.在培养的肾类器官的主要细胞分化轨迹中确定人类足细胞发育的WT1相关表观基因组景观
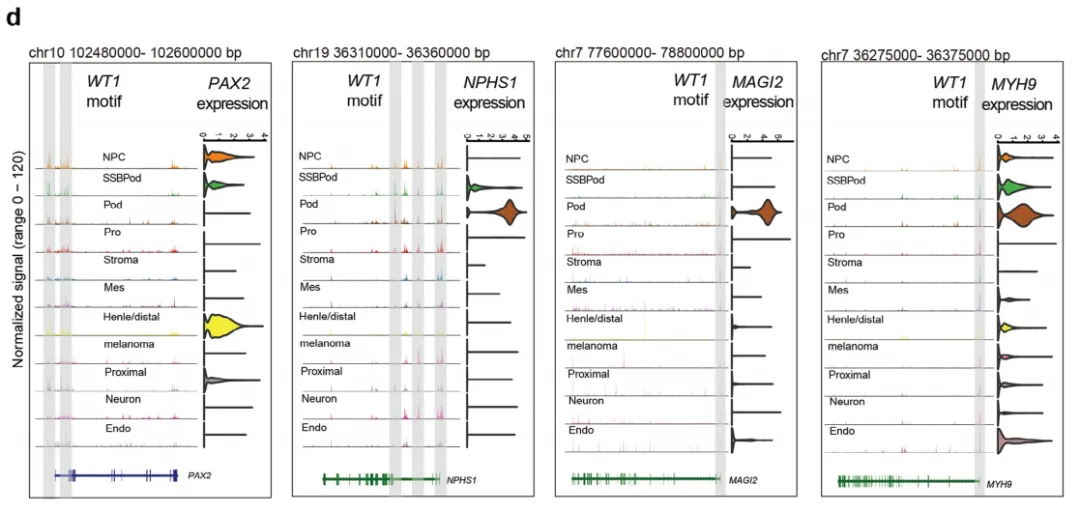
接下来,他们在体外培养了与胎儿肾脏发育相似的肾脏类器官,并进行相关图谱聚类分析。图2b显示,WT1基序开放活性评分和WT1的表达在NPC、SSBPod和足细胞簇中是特异性的,这证实了高度的一致性。从图2c~d可发现,在肾类器官足细胞发育过程中,WT1结合位点的全局分布变化可以忽略不计,主要位于基因启动子和假定的远端增强子,类似于胎儿肾脏;此外,WNT信号通路分子PAX2属于scRNA-seq序列在NPC/SSBPod簇中特异性表达,WT1基序位于PAX2启动子和增强子区域。并且在图2d中也能发现,细胞连接装配和肌动蛋白丝组织可以调节和维持足细胞特定的足状结构。细胞连接组装分子NPHS1、MAGI2和MYH9在足细胞簇中特异性表达,在其启动子和增强子区域发现WT1基序。总之,WT1相关的人类足细胞发育的表观基因组景观,也证实了肾脏和肾类器官之间的相似性。
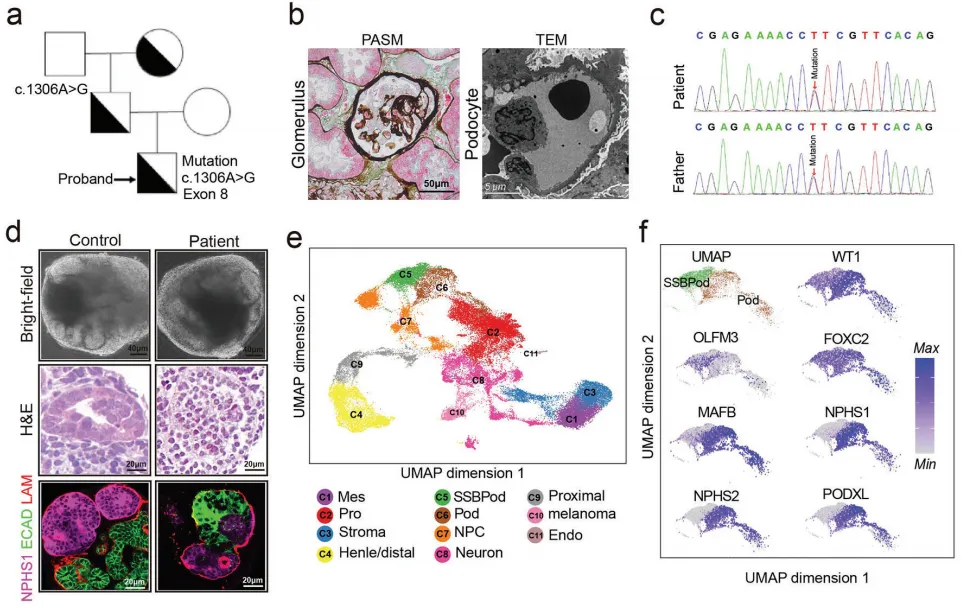
3.WT1突变诱导培养肾类器官SSBPod和足细胞的细胞过程失调
接下来,如图3a~b所示,他们从携带WT1突变的患者诱导多能干细胞(iPSCs)中提取培养的肾类器官来模拟足细胞表型,利用CRISPR-Cas9基因编辑技术,对携带WT1突变的iPSCs进行了基因校正,并在体外和体内条件下培养了携带WT1突变患者iPS的肾脏类器官。图3b的PASM染色和透射电镜均显示局灶节段性肾小球硬化和足细胞足突融合。通过图3c的测序分析发现c.1306A>G的杂合单核苷酸WT1突变,对照和患者的肾脏类器官均显示出包含足细胞的肾单位样结构。图3d显示,分化后,对照组和患者源性肾类器官均表现出含有足细胞的肾单位样结构。在图3d~k中,通过免疫荧光染色NPHS1(足细胞染色)、ECAD(肾小管染色)和LAM(基底膜染色)进一步验证肾类器官;通过scRNA-seq分析肾脏类器官的细胞组成,拟时序结果提示患者的足细胞发育延迟,GO分析导致足细胞发育迟缓的关键信号通路,并进一步分析信号通路的关键基因发现,足细胞发育标志物OLFM3的表达增加,而裂孔隔膜、WNT信号通路和细胞骨架的基因表达均降低。综上,结果揭示了患者源性肾类器官足细胞发育过程的延迟,以及患者源性肾类器官足细胞结构的缺陷。
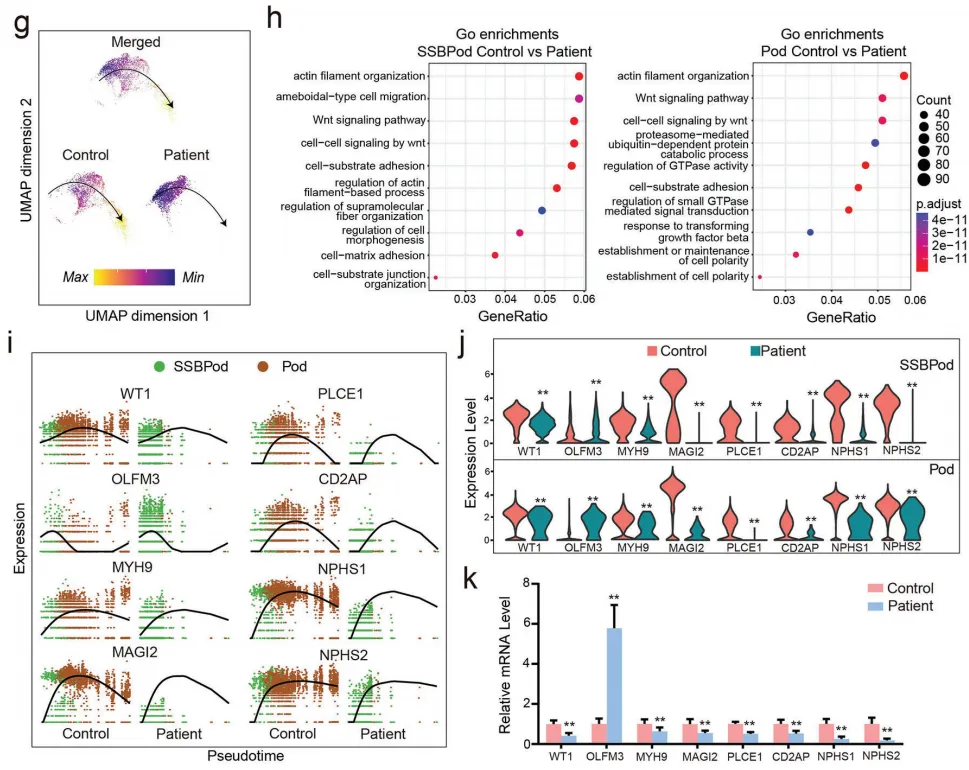
4.移植肾类器官足细胞中WT1突变导致的细胞过程失调
为了精确模拟成熟足细胞表型,如图4a所示,他们通过将类器官移植到肾被膜中来生成植入的肾类器官。对照组和患者源性肾类器官均表现出更成熟的肾小球结构。图4b~c显示,将肾脏类器官植入小鼠肾包膜下,可使肾小球滤过屏障成熟,荧光染色证实了植入后的肾脏类器官具有不同细胞成分。在图4d中,利用scRNA-seq分析植入后肾脏类器官,同样提示患者来源类器官的足细胞发育延迟。图4e~g显示,GO分析证实了WT1突变在足细胞发育和结构通路中的关键作用,该结果与体外培养阶段的分析非常相似。在患者样本中,足细胞发育标志物OLFM3的表达增加,而血管化通路、裂孔隔膜、WNT信号通路、细胞骨架和细胞黏附标志物的表达均降低。总之,在植入后肾脏类器官阶段,患者足细胞同样发育迟缓,足细胞结构存在缺陷,最终导致肾小球滤过屏障受损。
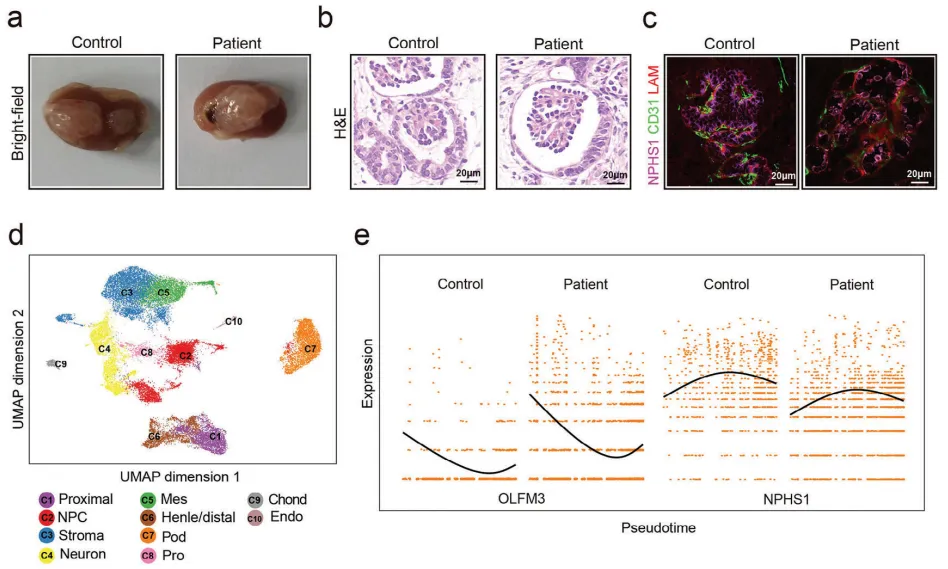
5.通过CRISPR/Cas9编辑携带WT1突变的患者来源的肾类器官,拯救足细胞表型
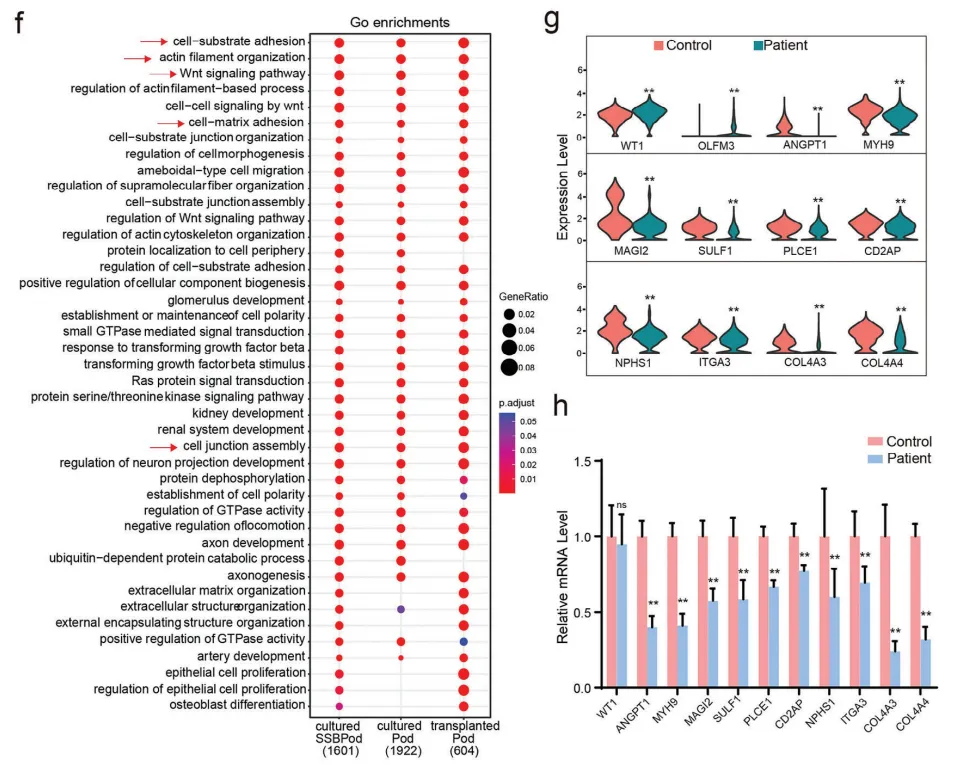
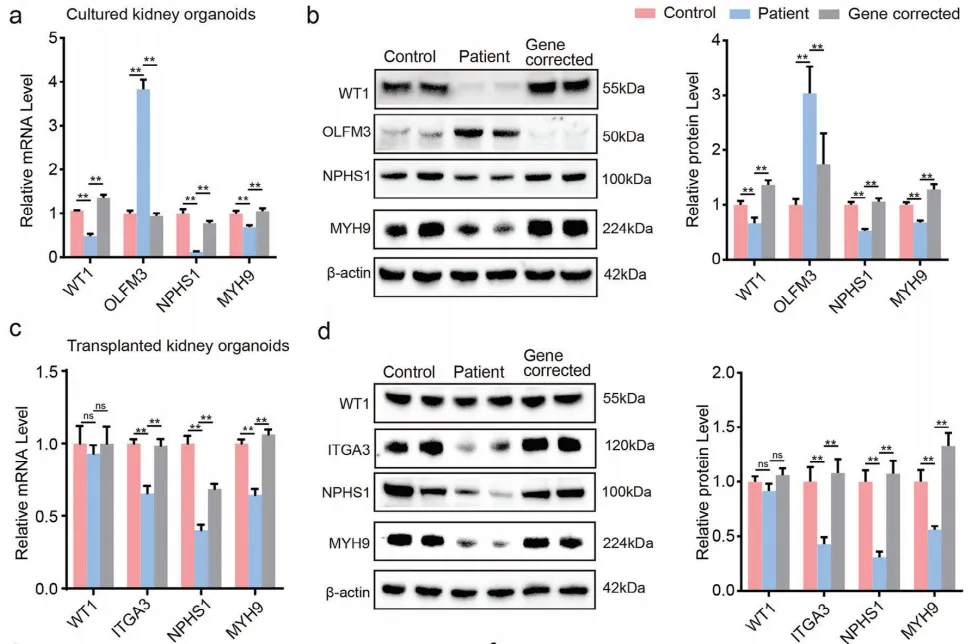
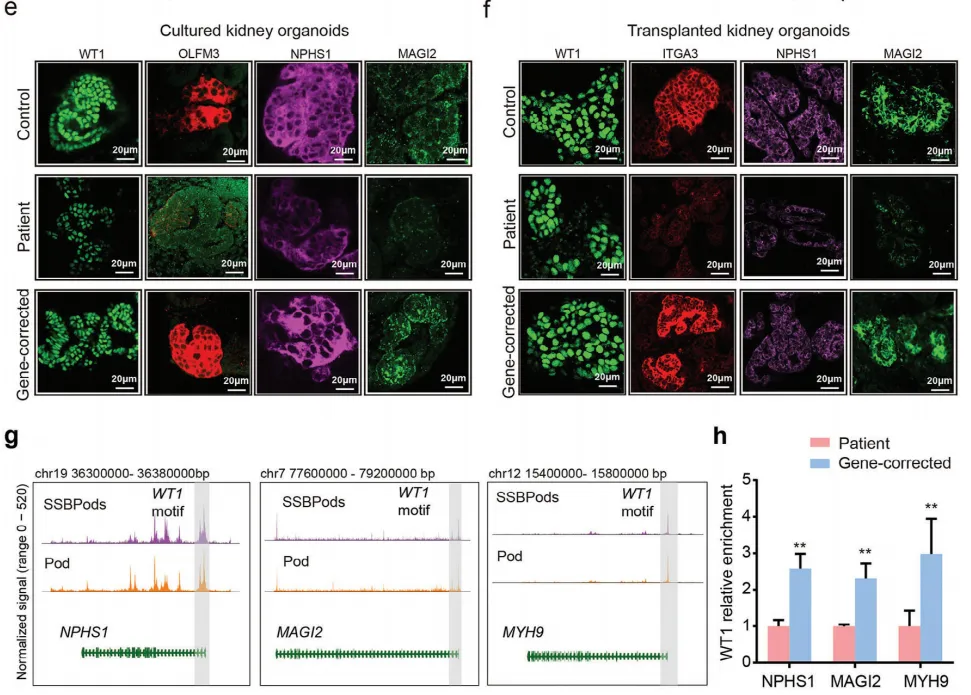
前面已证实c.1306A>G突变是该病的病因,因此他们接着通过CRISPR/Cas9基因编辑技术修复了突变。如图5a~b和图5e所示,在患者培养的肾类器官中,淤泥膜(NPHS1/MAGI2)、足细胞发育(OLFM3)和细胞骨架(MYH9)通路中基因的mRNA和蛋白水平明显改变,这些基因随后在基因校正的培养肾类器官中获救。此外,图5c~d和图5f显示,参与NPHS1/MAGI2、细胞基质粘附(ITGA3)和MYH9途径的基因的mRNA和蛋白质水平在患者来源的植入肾类器官中明显降低,这些基因在基因校正的植入肾类器官中也很容易恢复。图5g的scATAC-seq的基序分析也预测WT1与这三个基因的启动子位点结合。这三个基因位点的结合活性在患者源性肾类器官中均下降,而在基因校正后的肾类器官中恢复。此外,在图5h中发现,这些由WT1突变引起的表观基因组变化与观察到的基因表达变化一致。结果表明,培养和植入的肾类器官很好地模拟了足细胞的分子表型,这证明了WT1突变在表观基因组和转录组水平上的致病作用。
五、研究小结
该研究生成了胎儿肾脏和肾类器官的单细胞染色质可及性和基因表达图谱。WT1靶向基因对足细胞的发育及其结构的维持至关重要,包括调节WNT信号通路的BMPER/PAX2/MAGI2,维持肌动蛋白丝组织的MYH9和调节细胞连接组装的NPHS1。为了进一步说明WT1介导的转录调控在足细胞发育过程中的功能重要性,他们培养和植入了由WT1杂合错义突变患者的iPSCs衍生的患者源性肾类器官。scRNA-seq和功能分析的结果证实,由于WT1突变无法激活靶基因MAGI2、MYH9和NPHS1,因此会导致足细胞发育延迟并导致细胞结构损伤。值得注意的是,使用CRISPR-Cas9基因编辑纠正患者iPSCs中的突变可以挽救足细胞表型。总的来说,这项工作阐明了WT1与人类足细胞发育相关的表观基因组景观,并确定了WT1突变的致病作用,不仅为理解肾脏发育机制提供了新见解,也为肾脏疾病的研究和治疗提供了新的方向。
六、国自然中标情况

 文章推荐
文章推荐