新冠重大发现!哈佛医学院魏文毅团队等拿下中科院1区15.8分:揭示广谱抗冠状病毒新策略
2024-11-22 10:54:56
|
访问量:14122
2019年新冠疫情爆发后,虽然时间转眼过去几年,但是它的遗留效应仍然深远。那么关于新冠有什么课题设计思路呢?今天我们一起来探讨一下。
COVID-19是由严重急性呼吸综合征冠状病毒2(SARS-CoV-2)引起的呼吸道疾病,也就是曾经我们常常提起的新冠。SARS-CoV-2是一种正义单链RNA病毒,主要依赖其表面刺突(S)蛋白与宿主细胞受体血管紧张素转换酶2(ACE2)的相互作用侵染细胞。基于这一发现,既往已开发了多种手段来阻止SARS-CoV-2感染。此外,还成功研发并广泛使用了多种疫苗,在保护人群方面发挥了重要作用。
然而,新冠病毒持续变异,导致病毒逃逸免疫监测和疫苗产生的中和抗体。因此,迫切需要研发有效的抗病毒药物,以应对SARS-CoV-2不断出现的变种。
下面我们将分享一篇发表于中科院1区期刊Science Translational Medicine,影响因子为15.8的一篇高分文献,名为《USP2抑制在体外阻止ACE2依赖性冠状病毒的感染,并在小鼠中对SARS-CoV-2具有保护作用》,希望能给大家带来不一样的灵感。

【文章题目】:USP2抑制在体外阻止ACE2依赖性冠状病毒的感染,并在小鼠中对SARS-CoV-2具有保护作用
【发表期刊】:Science Translational Medicine
【发表日期】:2023.12
一、研究背景
①SARS-CoV-2是一种阳性单链RNA病毒,该病毒侵入人体是导致新冠肺炎的根本原因。②SARS-CoV-2主要依赖于其表面刺突(S)蛋白与宿主细胞ACE2的相互作用。③SARS-CoV-2在病毒基因组中的持续进化,从而使许多现有的COVID-19治疗方法无效。④鉴于ACE2在介导某些冠状病毒感染中的关键作用,阐明ACE2如何受到生理调控可能为针对ACE2依赖性病毒感染提供广泛的治疗策略。
二、技术路线
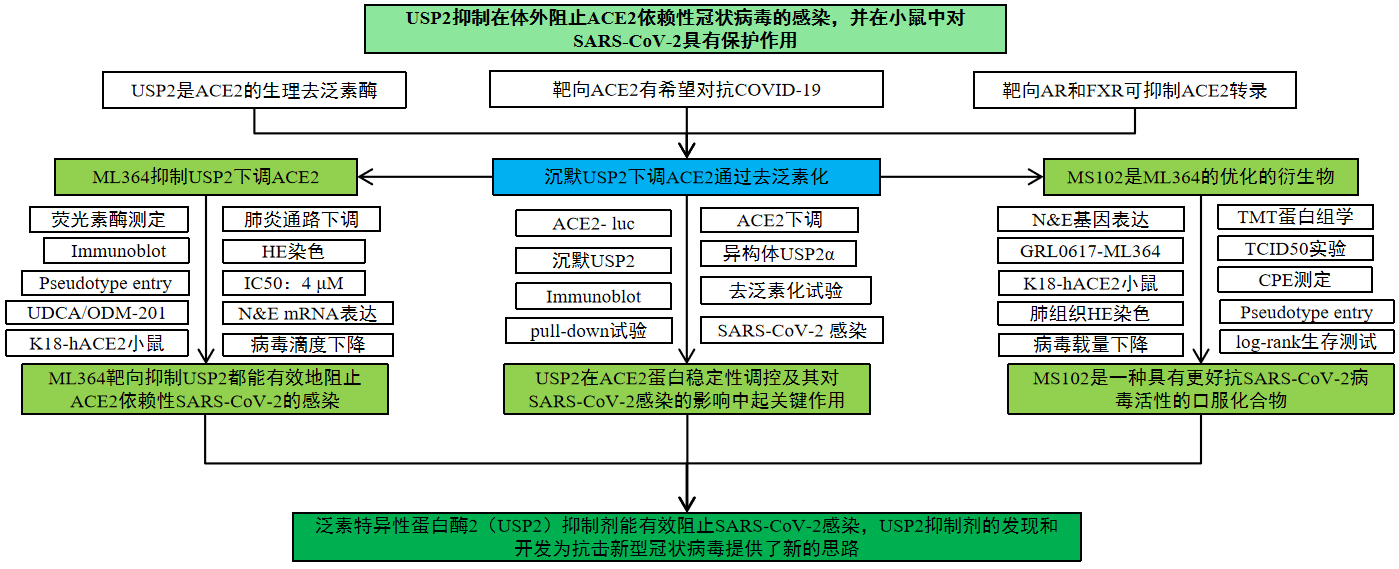
三、研究结果
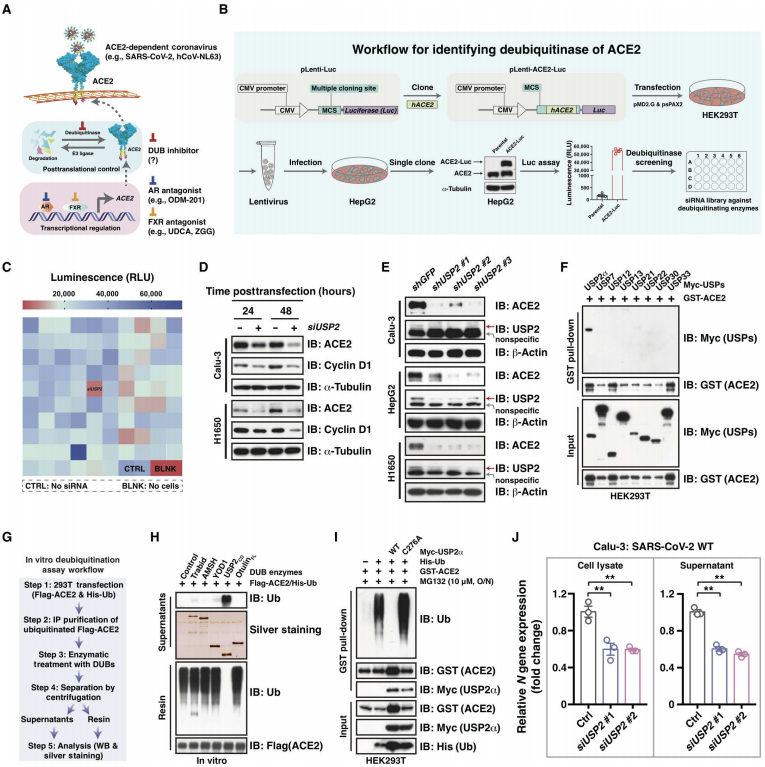
1.USP2作为ACE2的生理去泛素酶
鉴于ACE2在介导某些冠状病毒感染中的关键作用,作者对“ACE2是如何受到生理调控的”这一问题展开了探究。图1A显示,他们鉴定促进细胞中蛋白质存活的ACE2的去泛素酶(DUBs),可能为通过降低ACE2蛋白丰度来阻断SARSCoV-2感染提供了一种可行的方法。作者已经发现泛素-蛋白酶体途径在ACE2蛋白降解中起重要作用。通过对DUB的筛选,图1C结果发现USP2的沉默对ACE2和荧光素酶融合基因(ACE2-Luc)信号的减少最为显著。此外,图1D~E结果表明沉默USP2导致内源性ACE2蛋白丰度降低。一致地,图1F表明USP2的典型异构体,USP2α与ACE2存在相互作用,并且在图1G~H中可以看到其在体外介导去泛素化。此外,图1I中USP2α的催化失活突变体(C276A)未能去除细胞中ACE2的泛素部分,证实了USP2α在催化ACE2去泛素化中的关键作用。基于假病毒的抑制试验,图1J中,观察到沉默USP2后,SARS-CoV-2病毒进入Calu-3细胞显著减少。总之,USP2α在ACE2蛋白稳定性调控及其对SARS-CoV-2感染的影响中起关键作用。
2.ML364抑制USP2阻断ACE2依赖性冠状病毒感染接下来,作者探究了ML364是否会抑制USP2进而阻断ACE2依赖性冠状病毒的感染。图2A~C显示,用USP2特异性抑制剂ML364处理HepG2细胞导致内源性ACE2蛋白表达降低;此外,ML364处理导致多个细胞系中ACE2蛋白呈时间依赖性降低,暴露于ML364的细胞中异位表达的ACE2-luc呈剂量依赖性减少。图2D表明,与放线菌酮单独处理相比,添加ML364共同处理可加速HepG2和H1650细胞中ACE2的降解。同时,在图2E中,观察到在ML364处理的情况下,SARS-CoV-2假病毒进入细胞的明显减少,ML364的抗病毒作用可能是ACE2依赖性的。
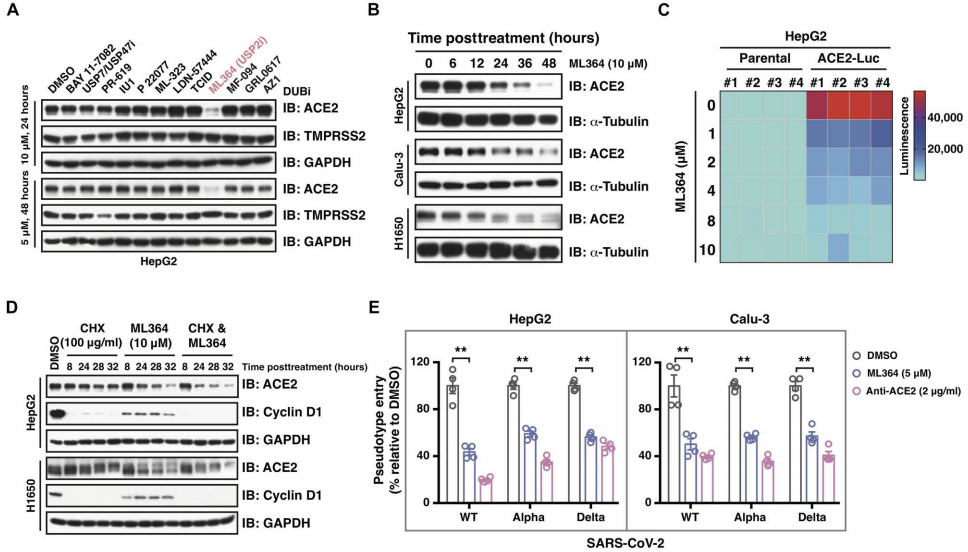
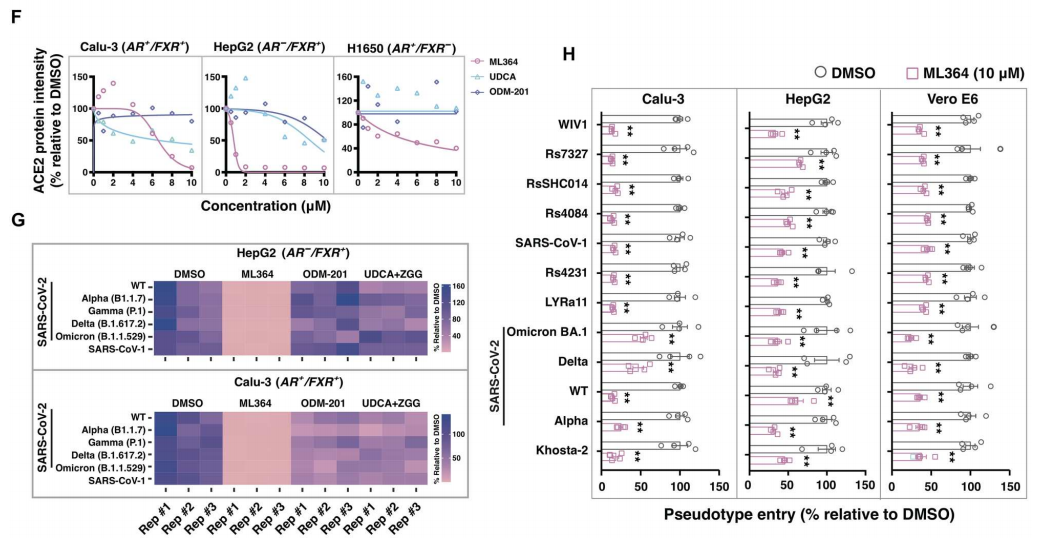
为了比较针对ACE2转录调控(AR和FXR)和翻译后调控(USP2)的抗病毒效果,评估了AR拮抗剂(ODM-201)、FXR拮抗剂(UDCA)和USP2抑制剂(ML364)的有效性。图2F显示,抑制USP2导致所有三种细胞系中ACE2蛋白降低,而UDCA仅轻度降低Calu-3和HepG2中的ACE2蛋白;AR拮抗剂降低的更少。在图2G~H中,与ACE2蛋白的减少一致,ML364处理在所有检测的细胞系中都阻止了SARS-CoV-2感染,而转录调控的影响较轻微;除SARS-CoV-2外,ML364也对其他依赖ACE2的病毒感染有影响。总之,ML364抑制USP2通过促进ACE2蛋白的降解有效减轻ACE2依赖性病毒感染。
3.ML364可在体外阻止SARS-CoV-2 WT及其变体的感染
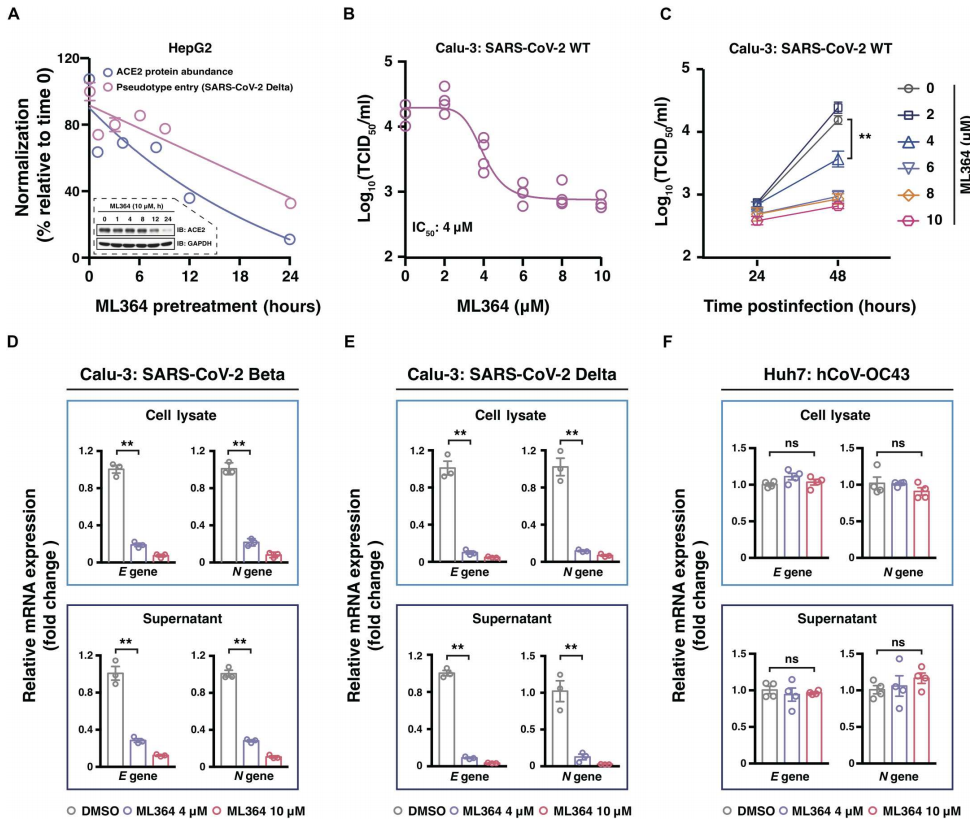
接着,作者研究了USP2抑制ACE2降解和SARS-CoV-2预防的动力学。从图3A中可以看到,在以HepG2为代表性模型中发现ML364处理12小时内,ACE2蛋白丰度下降了50%;表明ML364对USP2的抑制以ACE2依赖的方式阻碍了SARS-CoV-2进入细胞。此外,在图3B中可以确定ML364在Calu-3细胞中对真正的SARS-CoV-2的IC50约为4μM。图3C中,将ML364应用于Calu-3细胞发现SARS-CoV-2 WT的病毒复制随剂量增加而减少。用ML364处理Calu-3细胞导致广泛抑制各种真正的SARS-CoV-2变体,包括图3D的Beta变体和图3E的Delta变体。相反,在图3F中没有观察到ML364对hCoV-OC43的任何活性。综上,无论S蛋白如何突变,ML364靶向抑制USP2都能有效地阻止ACE2依赖性SARS-CoV-2的感染。
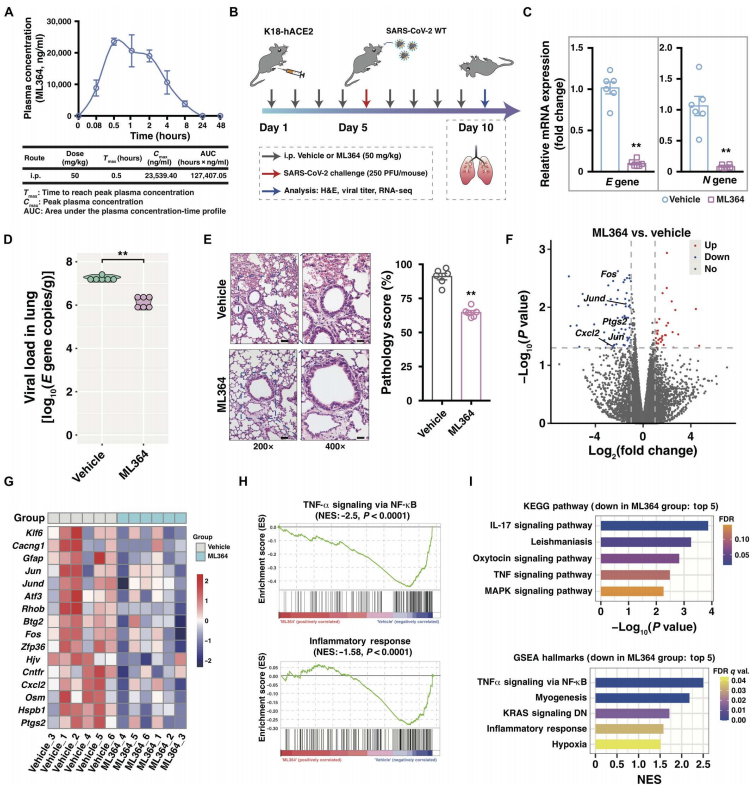
为了确定ML364在体内给药的安全和合适的剂量,作者给雄性C57BL/6小鼠进行了药代动力学测量。图4A显示,单次腹腔给药后的第30min时,观察到ML364的血药浓度峰值,表明其吸收迅速,暴露良好。此外,图4C~E显示给药后,小鼠肺中病毒E和N基因的产生减少,以及病毒载量显著下降;HE染色显示ML364处理的小鼠整体肺部病理减少。如图4F对肺组织进行RNA-seq后,可以看到ML364给药在体内没有引起大范围的基因表达变化,进一步表明了给药的安全性。然而,图4G~I的GSEA和KEGG富集分析显示,ML364处理小鼠的肺部炎症反应信号下调最为显著,这与ML364处理小鼠的病毒载量降低一致。总之,以上实验结果支持了ML364作为预防SARS-CoV-2感染的候选药物的可行性。
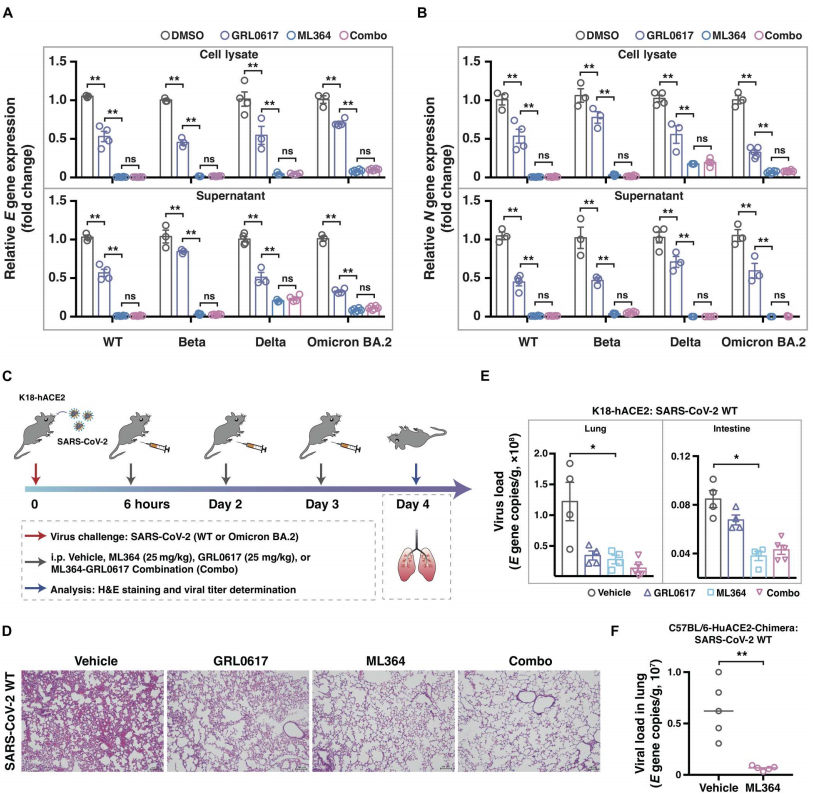
4.治疗性给药ML364可降低体外和K18-hACE2小鼠的SARS-CoV-2病毒载量
为了进一步评估ML364在SARS-CoV-2感染中的治疗潜力,作者用真正的SARS-CoV6-2WT和几种当代变体感染Calu-3细胞,接触PLpro抑制剂GRL0617、ML364或GRL0617-ML364组合(Combo)感染48小时。图5A~B可以看到ML364单独或与GRL0617联合对所有SARS-CoV-2病毒均有效,包括WT、Beta变异、Delta变异和Omicron BA.2亚谱系。此外,在图5C中,使用K18-hACE2转基因小鼠模型在体内测试了这些治疗方案。与细胞培养模型结果一致,图5D~E显示SARS-CoV-2感染后6小时给予ML364改善了肺部病理,小鼠的肺和小肠中病毒滴度和SARS-CoV-2基因表达的降低支持了这一点。此外,他们利用另外两种hACE2转基因小鼠模型对ML364治疗SARS-CoV-2感染的疗效进行了深入研究,图5F结果表明ML364在两种小鼠模型中都显示出巨大的治疗潜力。综上,ML364通过抑制USP2并随后降低ACE2蛋白,在体外和体内都有效地抵消了SARS-CoV-2感染。并强调了ML364作为对抗SARS-CoV-2的有希望的治疗候选药物的潜力,无论病毒如何变异。
5.MS102是USP2抑制剂的口服形式,具有改善的药代动力学和抗病毒活性
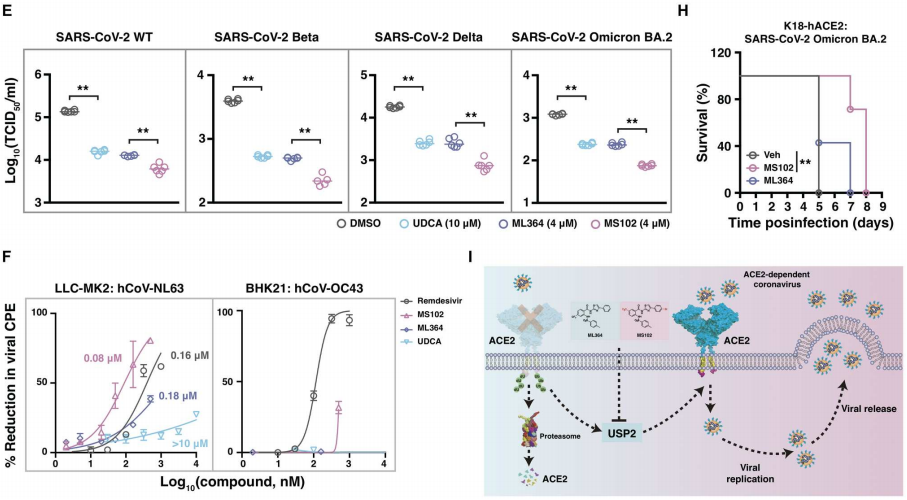
通过前面的实验,作者已经确定USP2抑制剂可以抵抗SARS-CoV-2感染。但如图4A所示,选用的ML364药代动力学竞争力不强。因此设计合成了约90个ML364衍生物,发现图6A中一种特殊的化合物MS102是其中的首选。图6B的蛋白组学分析发现ML364和MS102这两种化合物具有相似的蛋白质还原谱。可以从图6C中看到,与降低ACE2蛋白稳定性的能力增强一致,MS102在阻断原发SARS-CoV-2 WT感染人支气管上皮细胞方面表现出更高的功效。图6D中MS102的活性增强在所有测试的ACE2依赖假型中都被观察到。此外,图6E~F显示,在比较UDCA、ML364和MS102这三种化合物对SARS-CoV-2感染Calu-3细胞的抑制时,MS102表现出更强的活性;进一步,观察到ML364和MS102都能有效抑制ACE2依赖性冠状病毒hCoV-NL63,而在评估浓度下,它们对ACE2非依赖性菌株hCoV-OC43表现出有限或没有活性。
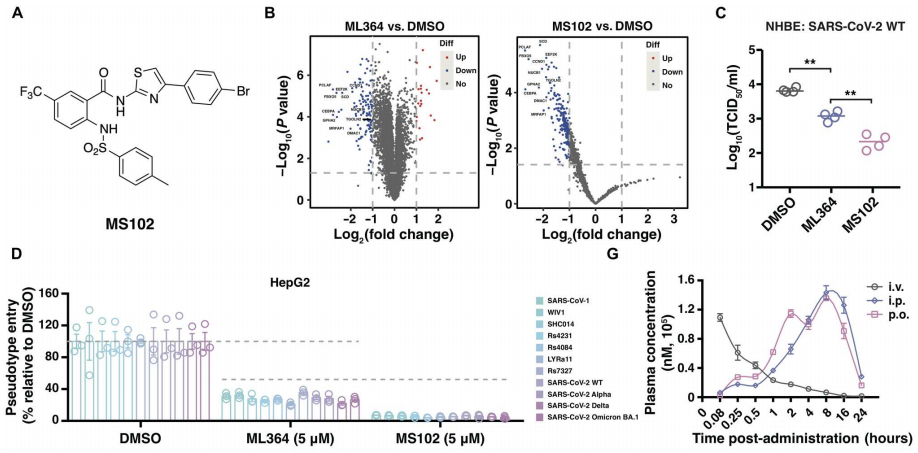
最后,在图6G中作者惊讶地发现MS102的口服生物利用度接近100%,突出了其作为未来临床应用的口服治疗候选药物的潜力。并且,可以从图6H中看到,在评估ML364和MS102感染SARS-CoV-2 Omicron BA.2亚谱系后促进K18-hACE2转基因小鼠存活的有效性中,MS102处理的小鼠表现出明显增强的结果。总之,如图6I所示,这些发现证实MS102是一种具有更好抗病毒活性的口服化合物,证实了通过抑制USP2靶向ACE2的翻译后控制是一种广泛而有效的治疗ACE2依赖性冠状病毒的方法。
四、研究小结
该研究报告了USP2是一种宿主导向的抗病毒靶点,并且进一步研发了一种可以口服的USP2抑制剂MS102,它对ACE2依赖的冠状病毒表现出有效的抗病毒活性。USP2是ACE2的去泛素化酶,通过特异性小分子靶向抑制降低ACE2蛋白水平。研究结果表明分子抑制剂ML364可导致ACE2蛋白丰度显著且可逆性降低,从而阻断试验中检测的各种ACE2依赖性冠状病毒。通过利用人类ACE2转基因小鼠模型,研究团队进一步通过减少病毒载量和减轻肺部炎症证明了ML364可有效控制SARS-CoV-2感染引起的疾病。此外,还证明了MS102在体内具有良好的药代动力学特性和抗病毒活性,有望进一步发展成为治疗依赖ACE2的病毒感染的抗病毒手段。
五、国自然中标情况













 文章推荐
文章推荐