
2.SCI信息

外泌体是由细胞产生的细胞外囊泡,它们携带着核酸、蛋白质、脂质和代谢物。这些囊泡作为健康与疾病状态下的近距离及远距离细胞间通讯的介质,对细胞生物学的各个层面产生影响。那么关于外泌体有什么课题设计思路呢?今天我们一起来探讨一下。
今天我们将分享一篇发表于中科院1区期刊Journal of Nanobiotechnology,影响因子为10.6的文献,希望能给大家带来不一样的灵感。
一、课题挂靠与SCI信息
1.课题挂靠

2.SCI信息

【文章题目】:人类脂肪间充质干细胞的外泌体通过靶向PI3K/AKT轴改善自闭症谱系障碍小鼠模型的神经发生和自闭症谱系障碍样行为
【发表期刊】:Journal of Nanobiotechnology
【影响因子】:10.6
【发表日期】:2024.2
二、研究背景
①外泌体含有lncRNA,在自闭症谱系障碍(ASD)个体的神经发生调节中发挥关键作用;
②大多数ASD大脑表现出常见的lncRNA失调模式,如PTCHD1AS 1-3、SHANK2-AS和BDNF-AS;
③ASD的核心症状是社交障碍、沟通障碍和重复刻板行为障碍,这是一种异质性发育障碍;
④近期研究表明,从胎儿肝脏移植造血干细胞(hsc)有助于缓解儿童ASD样症状。
三、技术路线
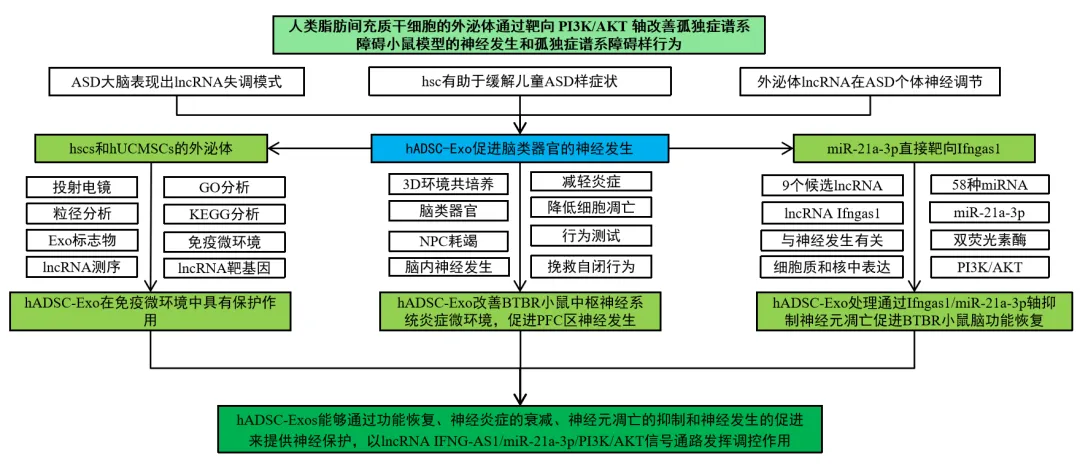
四、研究结果
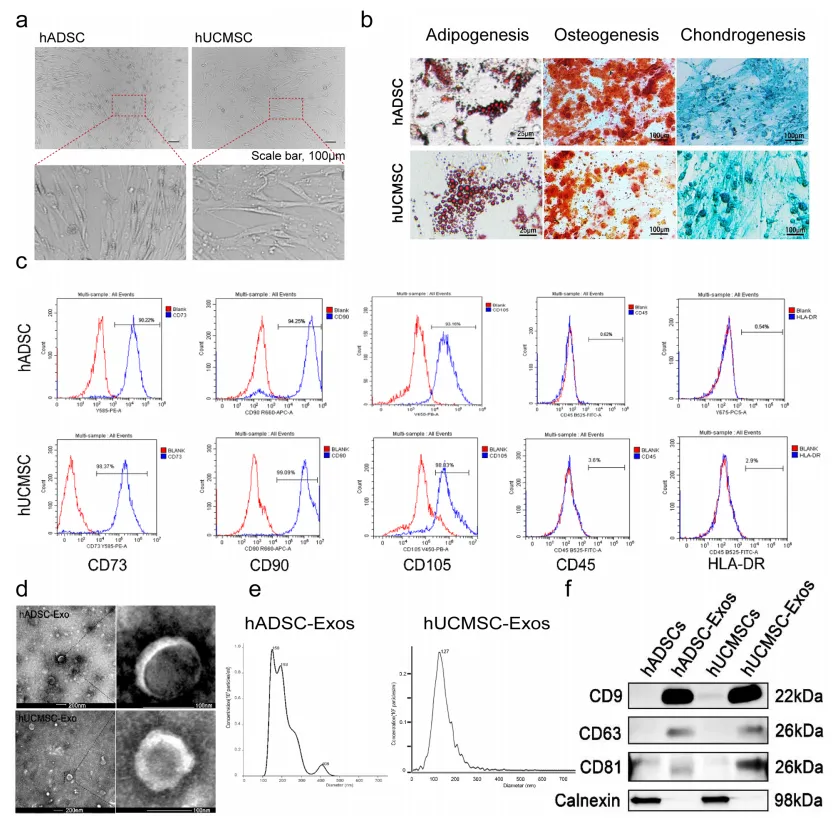
1、hADSC和hUCMSC衍生外泌体的表征
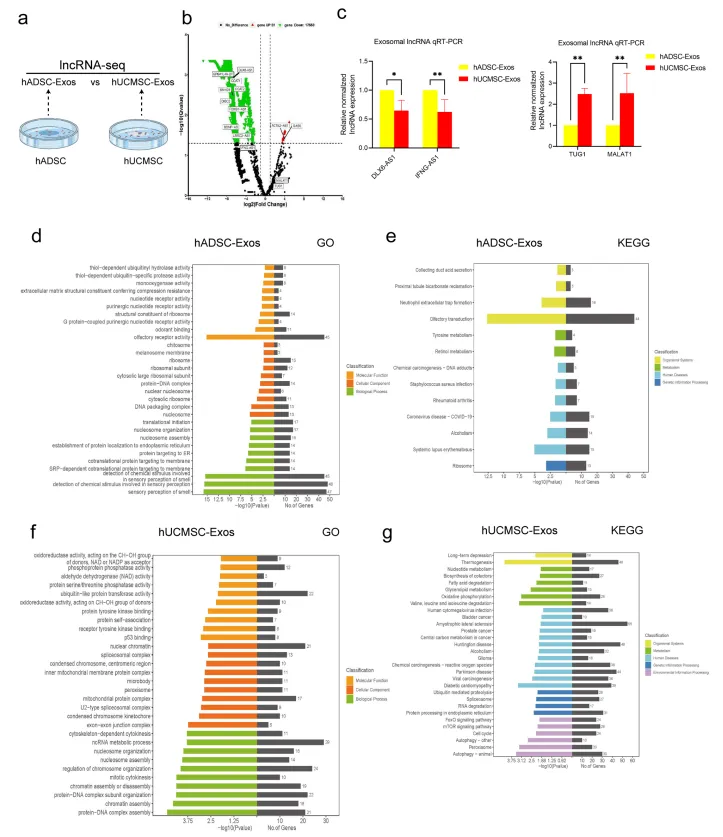
2、LncRNAs测序分析鉴定hADSC-Exo和hUCMSC-Exo
为了探索hADSC-Exo和hUCMSC-Exo之间的异同,经图2a~b的外泌体lncRNA测序发现BDNF-AS(lncRNA失调模式之一)等lncRNA在hADSCs-Exo中的表达更高;GAS5等lncRNA在火山地块的hUCMSC-Exo中表达较高。图2c的qRT-PCR结果显示,lnc-TUG1和MALAT1在hUCMSC-Exo中的表达高于hADSC-Exo。此外,图2d~g的GO分析、KEGG通路分析显示,差异表达基因(DEG)与核苷酸受体活性和翻译起始显著相关;类风湿性关节炎、酒精中毒和核糖体是上调基因的主要通路;DEG显著参与醛脱氢酶(NAD)活性和ncRNA代谢过程;缬氨酸、亮氨酸和异亮氨酸的降解和细胞周期是上调基因的主要途径。以上结果表明hADSC-Exo在免疫微环境中具有保护作用。
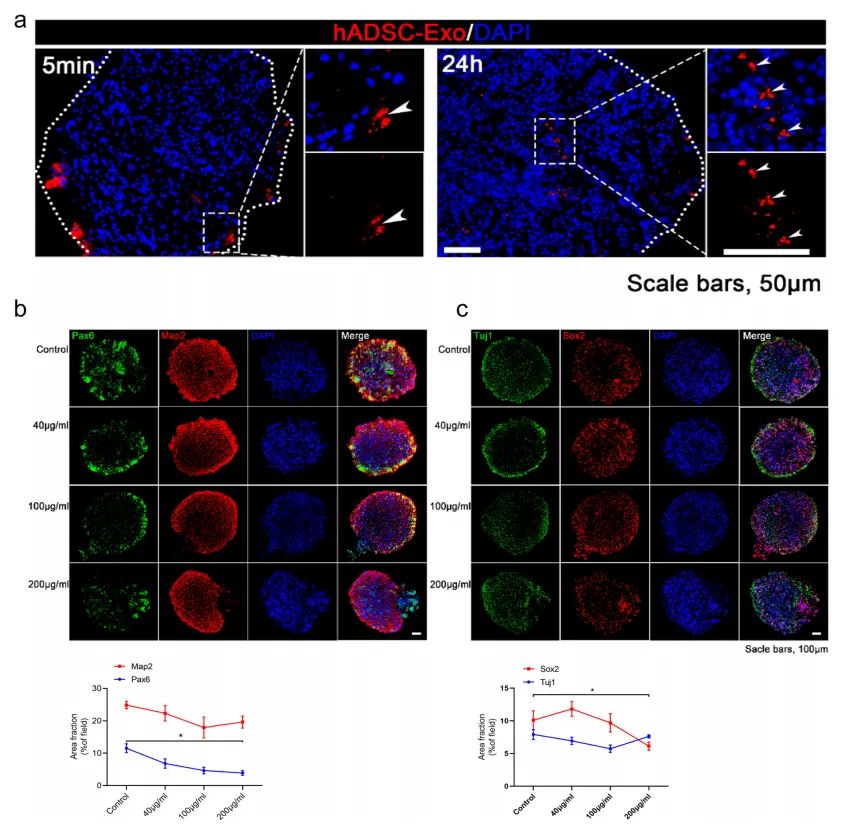
3、hADSC-Exo抑制神经干细胞(NSC)的增殖,并倾向于促进脑类器官的神经发生
4、hADSC-Exo可以调节BTBR小鼠神经发生和脑炎症相关基因的表达
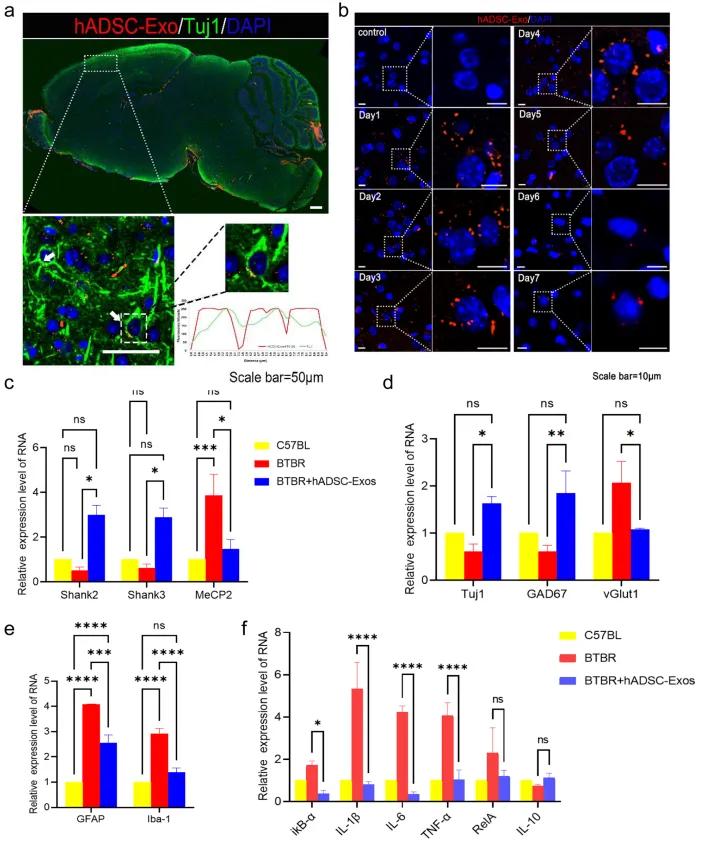
BTBR小鼠(BTBR T+tf/J)是应用最广泛的ASD近交系小鼠模型之一。用PKH26标记,然后选择脑室内(ICV)输注hADSC-Exo。图4a~b的共定位表明,在BTBR小鼠的皮层神经元中可以测量到hADSC-Exo,且在BTBR小鼠体内的滞留时间为7天。图4c~d显示,在BTBR小鼠中检测了ASD标记基因Shank2、Shank3、MeCP2的表达,hADSC-Exo干预后,BTBR小鼠的ASD标记基因发生逆转,与WT相比趋于正常化;此外,BTBR小鼠中Tuj1、GAD67、vGLU1等神经元基因的表达也被hADSC-Exo干预逆转。在图4e中,GFAP和Iba-1表达水平升高,被认为与BTBR小鼠脑内炎症有关。图4f的RT-PCR实验证明hADSC-Exo可有效改善脑内微环境,减轻炎症。综上,hADSC-Exo不仅改善了BTBR小鼠脑内神经发生,而且改善了兴奋性和抑制性神经传递的失衡。
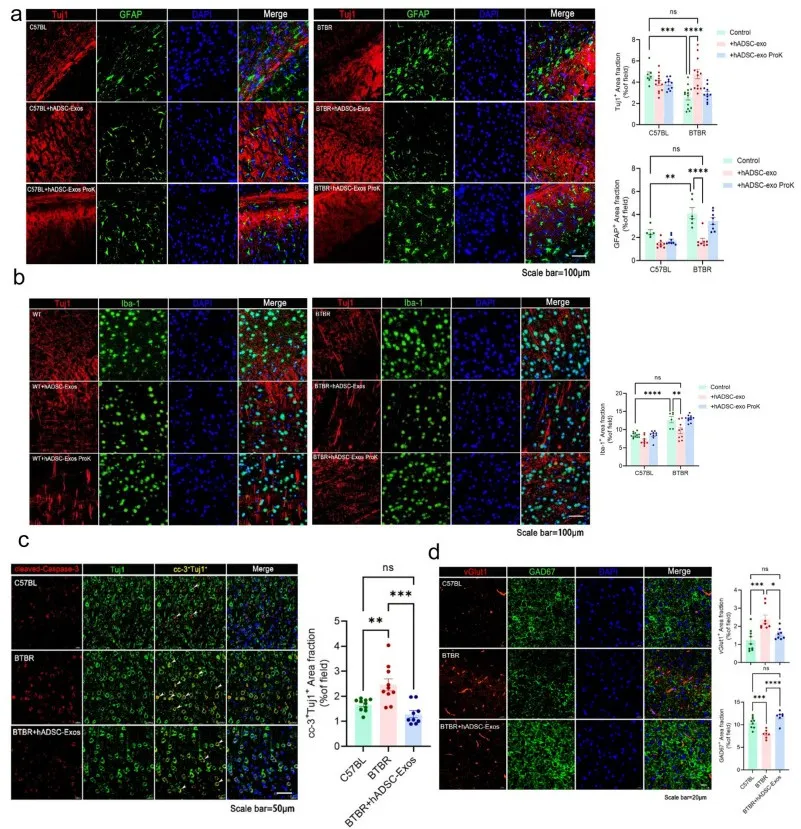
5、hADSC-Exo治疗可改善BTBR小鼠大脑PFC区域的炎症并促进神经发生
为了验证hADSC-Exo是否在体内影响星形胶质细胞和小胶质细胞的活化,他们开展了进一步实验。图5a~b显示,hADSC-Exo处理后,神经元数量明显增加,星形胶质细胞和小胶质细胞的活性明显降低;与未处理的BTBR小鼠相比,神经元的百分比显著增加了两倍,但BTBR小鼠的GFAP+细胞数量急剧减少1.6倍,Iba-1+细胞数量急剧减少2倍。此外,从图5c~d可看出,hADSC-Exo处理后,BTBR小鼠前额叶皮质(PFC)中CC-3+细胞水平降低,同时,vGlu1+细胞增加2.1倍,GAD67+细胞减少2倍。这些结果表明hADSC-Exo可改善BTBR小鼠中枢神经系统炎症微环境,促进PFC区神经发生。
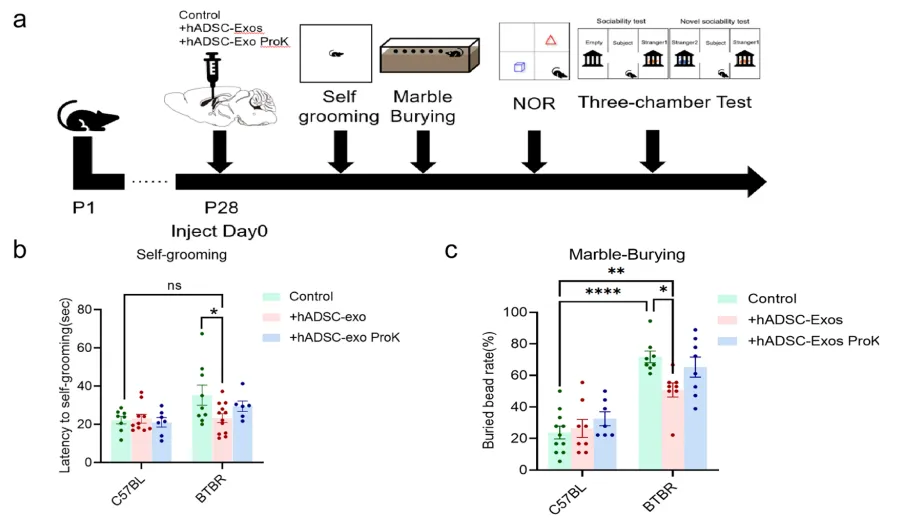
6、hADSC-Exo可逆转BTBR小鼠的ASD样行为
为了进一步验证hADSC-Exo对皮质神经元功能的影响,他们对BTBR小鼠进行了一系列ASD核心行为测试。首先,采用自我梳理测试来验证hADSC-Exo治疗是否影响刻板重复行为。图6b显示,与C57BL WT小鼠相比,hADSC-Exo治疗的BTBR小鼠表现出较短的自我梳理时间,且趋于正常化。同样,在图6c的弹珠掩埋试验中,BTBR小鼠比C57BL WT小鼠掩埋的弹珠更多,hADSC-Exo处理后逆转。而在图6d的新物体识别测试中发现,BTBR小鼠对新物体的识别能力下降,hADSC-Exo处理后,BTBR小鼠对新旧物体的偏好差异不再存在,这表明认知功能增加。图6f的三室测试发现BTBR小鼠对与陌生小鼠的互动不感兴趣,hADSC-Exo可恢复BTBR小鼠的社交能力。同时,图6g显示,经hADSC-Exo处理的BTBR小鼠对与不熟悉的小鼠#2互动表现出更大的兴趣。这些数据表明,hADSC-Exo可能会挽救BTBR小鼠的自闭症行为,如刻板行为、视觉识别记忆下降、社交能力下降和视觉识别记忆下降。
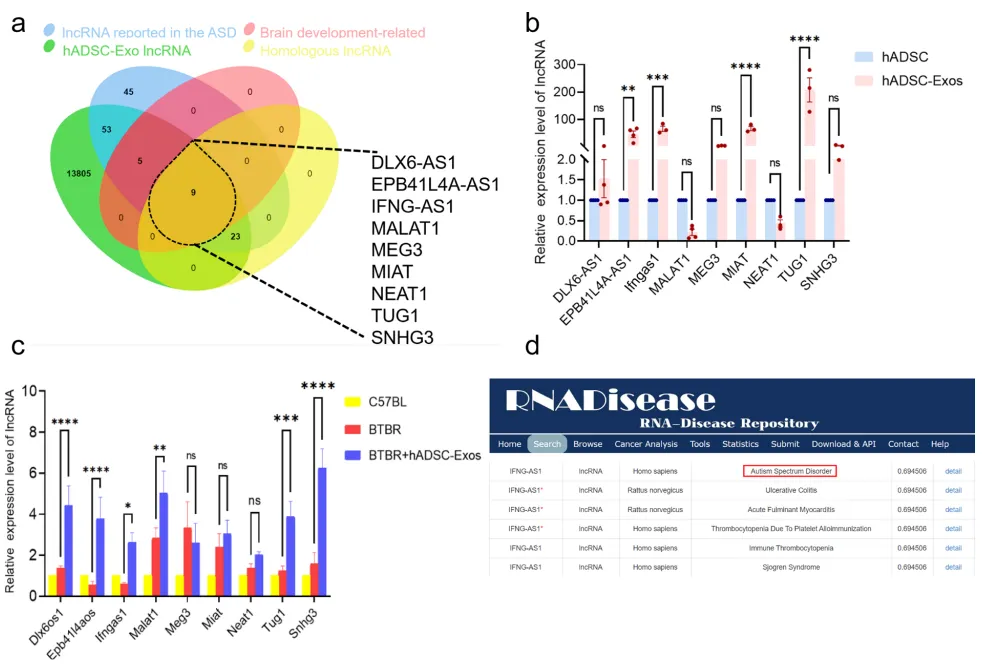
7、在hADSC-Exo中,lncRNA IFNGAS1已被确定与ASD显著相关
为了鉴定ASD的关键基因,他们通过生信分析,筛选了9个候选lncRNA。其中有3个lncRNA基因表达较高,如图7b的Epb41l4aos、Ifngas1和MIAT。图7c显示,hADSC-Exo处理后,lncRNA Ifngas1和Epb41l4aos的异常表达立即恢复到正常状态。经文献调研发现Ifngas1更有研究价值。通过图7d的FISH检测到该蛋白在不同亚细胞区室中的存在。这提示Ifngas1的表达可能与神经发生有关。且从图7e可看出,Ifngas1在细胞质和细胞核中均有表达。因此,Ifngas1被鉴定是可能在ASD生物网络中发挥关键作用的关键lncRNA。
8、Ifngas1可能作为miR-21a-3p的分子海绵,从而负向调控AKT信号通路
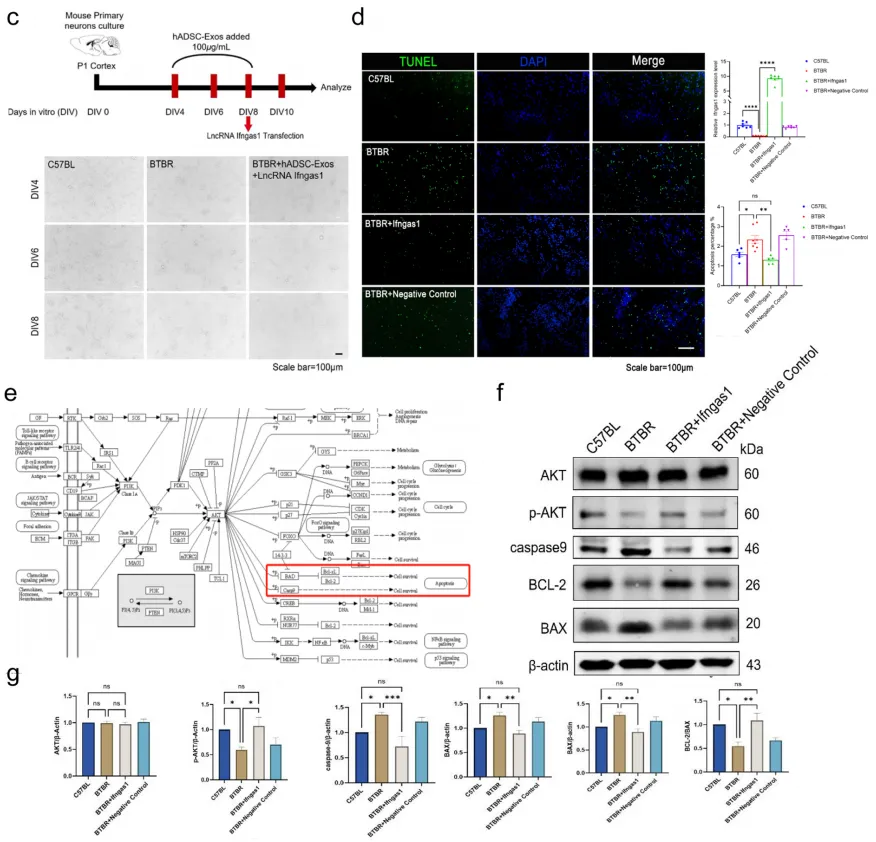
既往研究发现,ASD大脑中有58种miRNA与健康大脑中存在差异表达。其中,如图8a所示,miR-21a-3p在不同小鼠皮层中的表达差异显著,且在WT小鼠皮层中,其表达量比BTBR小鼠高7倍。图8b~d显示,miR-21a-3p直接靶向Ifngas1;Ifngas1过表达hADSC-Exo处理后,BTBR小鼠培养的皮质神经元轴突生长明显增强;Ifngas1可挽救BTBR小鼠皮质神经元的凋亡。此外,图8e~g显示,miR-21a-3p已被报道通过PI3K/AKT信号通路抗凋亡,WB结果显示,BTBR小鼠caspase9升高,AKT磷酸化降低,AKT可直接调控PI3K/AKT信号通路中的BCL-2和BAX;而Ifngas1逆转了此现象。这些结果证实hADSC-Exo处理通过Ifngas1/miR-21a-3p轴抑制神经元凋亡促进BTBR小鼠脑功能恢复。
五、研究小结
该文章证明了hADSC-Exos能够通过功能恢复、神经炎症的衰减、神经元凋亡的抑制、体外和体内神经发生的促进来赋予神经保护。hADSC-Exos衍生的lncRNA IFNG-AS1作为分子海绵,通过miR-21a-3p/PI3K/AKT信号通路促进神经发生,从而发挥调节作用。此发现为自闭症患者提供了一条潜在的治疗途径。
六、国自然中标情况

 文章推荐
文章推荐