
今天的文章我们将综合、详细地介绍细胞的各种死亡机制。

一、细胞死亡的定义
2005年第一届细胞死亡学术命名委员会对细胞死亡做出了较为清晰的定义,将细胞死亡定义为不同于濒死细胞的可逆细胞状态,死亡细胞是指细胞到达生命终点,处于不可逆转的状态。
二、细胞死亡的研究时间线
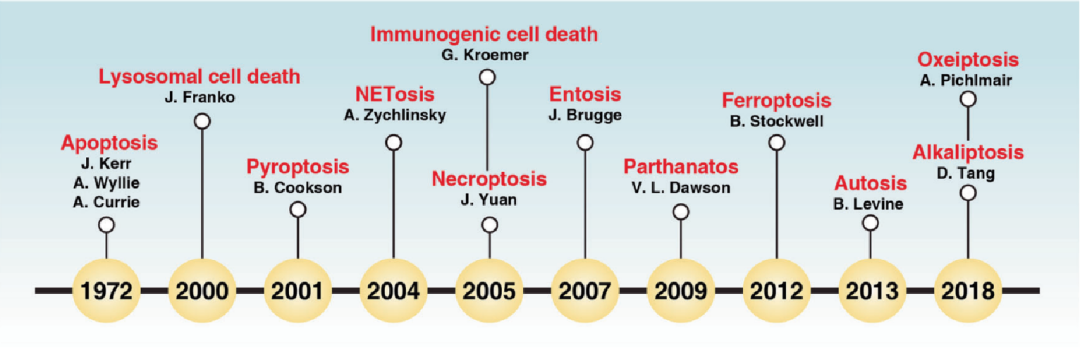
1972年Kerr等三位科学家首次提出了细胞凋亡的概念,2000年J·Franko提出了溶酶体介导的细胞死亡,然后就是细胞焦亡、中性粒细胞的炎性细胞死亡、坏死性凋亡、免疫原性细胞死亡、细胞侵入性死亡、依赖性细胞死亡、铁死亡、自体死亡(也就是自噬)、碱死亡、氧死亡以及近几年发现的铜死亡。
三、细胞死亡的分类
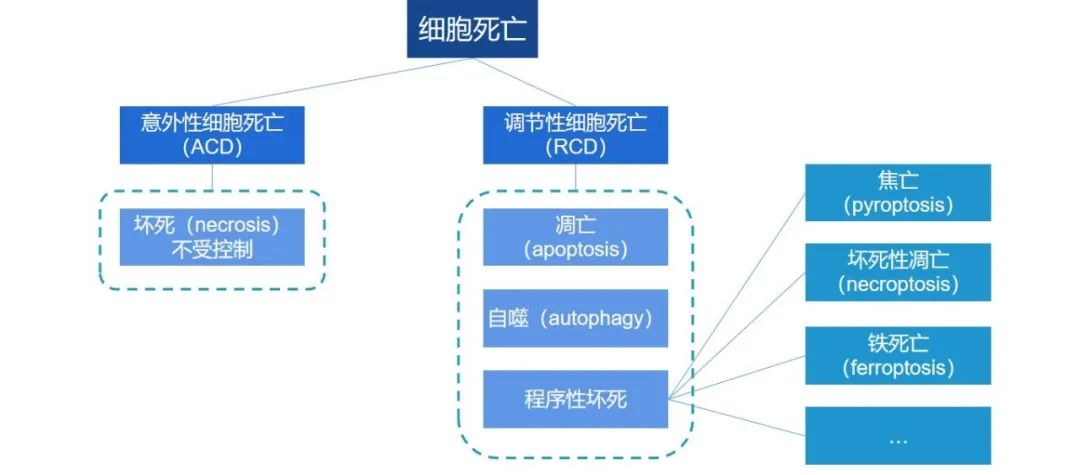
意外性细胞死亡和调节性细胞死亡,即ACD和RCD。ACD主要是指细胞坏死,是不受控制的,而RCD可以分为细胞凋亡、细胞自噬以及程序性坏死这三种类型,其中程序性坏死又包括细胞焦亡、坏死性凋亡、铁死亡等等。
四、各种细胞死亡的机制
01 细胞凋亡
细胞凋亡是细胞一种生理性、主动性的“自觉自杀行为”,是机体在生理或病理条件下,为了维持自身内环境稳态,通过基因调控而产生的主动、有序的细胞死亡,其主要形态特征是凋亡小体的形成。
细胞凋亡主要分为外源性细胞凋亡和内源性细胞凋亡:
外源性细胞凋亡是由死亡受体配体的加入或依赖性受体配体的退出引起的。CASP8和CASP10可以使死亡受体介导的外源性细胞凋亡;而CASP9则可以逆转这一过程。
DNA损伤、缺氧和代谢应激等因素可诱导内源性细胞凋亡;其中MOMP和线粒体蛋白质(例如CYCS)起到重要的调控作用。
CASP3、CASP6和CASP7被认为是外源性和内源性细胞凋亡的共同效应因子。
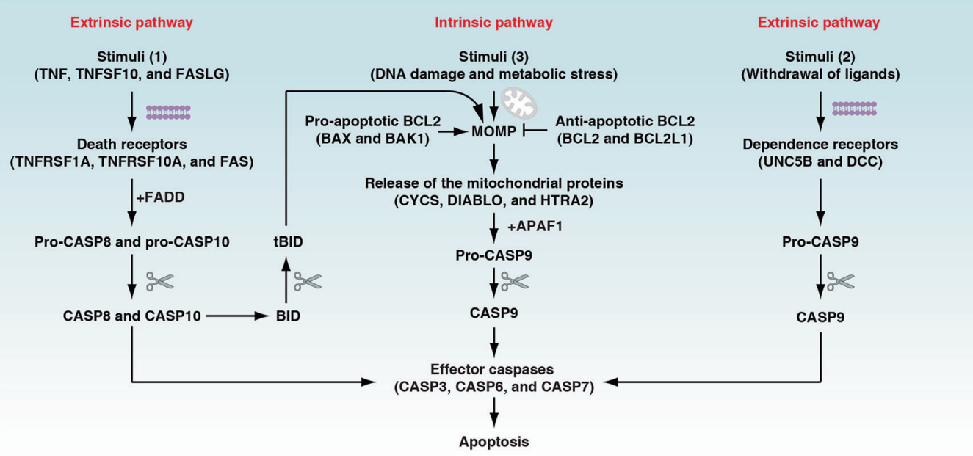
细胞凋亡的过程大致可分为以下几个阶段:首先是接受凋亡信号,然后是凋亡调控分子间的相互作用,紧接着是蛋白水解酶的活化(Caspase),最后细胞进入连续反应过程。
02 细胞自噬
细胞自噬是由自噬分子机制驱动的一种RCD,其特征是自噬空泡化。有些受损的蛋白质或细胞器被双层膜结构的自噬小泡包裹,降解到溶酶体(动物)或液泡(酵母和植物)中并回收。
自噬是溶酶体吞噬细胞器和其他内容物,以清除不必要或功能失调的成分的过程。通过自噬,生物体能完成细胞材料的系统降解和回收。
细胞自噬的机制为:Tat-Beclin 1诱导自噬依赖性细胞死亡的发生,该分子是一种自噬诱导肽,融合了BECN1和HIV Tat的蛋白氨基酸。这一过程可以通过阻断Tat-Beclin 1上游的Na+/K+-ATP酶来抑制。
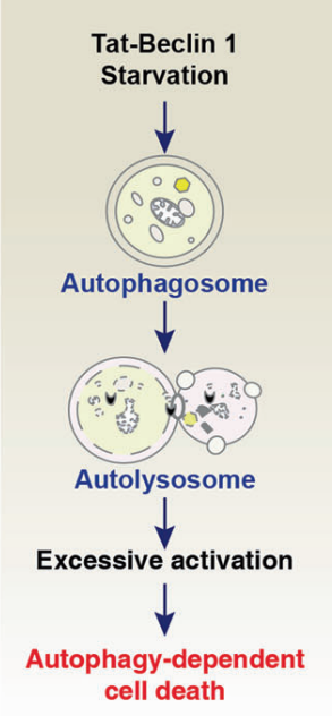
自噬依赖性细胞死亡可能在神经毒性和缺氧缺血诱导的神经元死亡中起重要作用,因此这种类型的RCD可能可以作为神经保护的靶点。
03 坏死性凋亡
在坏死性凋亡这一过程中,RIPK3激活MLKL是关键调节通路。上游诱导因子死亡受体(DR)、TLR或病毒分别通过RIPK1、TICAM1和ZBP1诱导RIPK3的激活。另外,粘附受体(AR)通过一种未知的适配蛋白或激酶激活RIPK3。
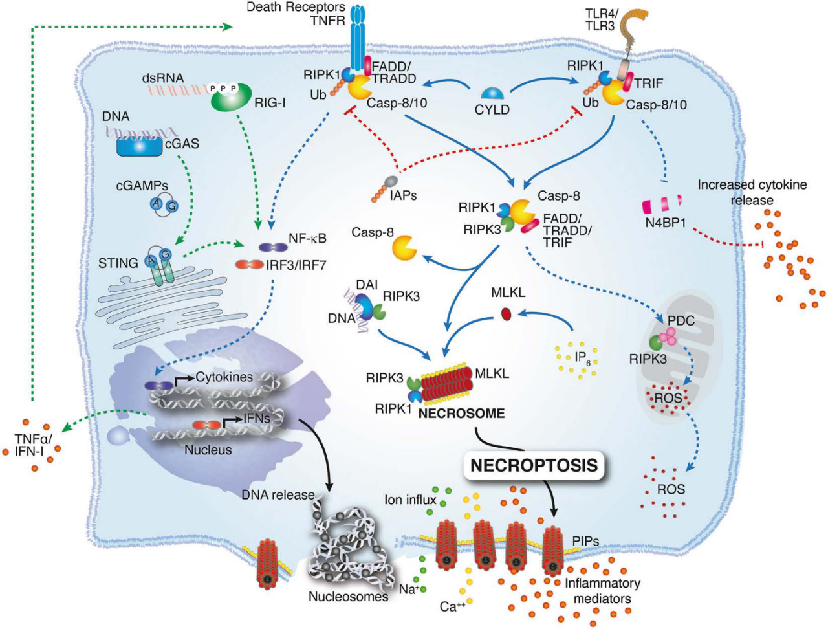
此外,RIPK3也可以不依赖于其激酶活性和MLKL,在细胞凋亡和NLRP3-炎性体活化和焦磷酸化中起调节作用。
04 细胞焦亡
细胞焦亡是由炎性小体激活的一种RCD形式,在炎症和免疫中起着重要的作用。
炎性小体可以分为典型的CASP1依赖性炎症小体和非典型的CASP11依赖性炎症小体:
典型的CASP1依赖性炎症小体可以被病原体相关分子模式(PAMPs),损伤相关分子模式(DAMPs)或其他免疫反应选择性激活。
非典型的CASP11依赖性炎症小体由巨噬细胞、单核细胞或其他细胞细胞质中的LPS激活,该过程不依赖细胞膜的TLR4受体。
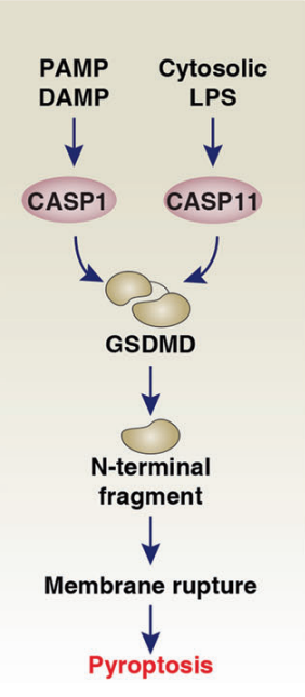
GSDMD被CASP11或CASP1切割产生22kDa C-末端片段(GSDMD-C)和31kDa N-末端片段(GSDMD-N);GSDMD-N产生后立即移位到质膜的内部小叶与磷脂结合,诱导孔的形成,最终导致细胞膜裂解,而GSDMD-C抑制GSDMD-N的这一活性。
05 铁死亡
铁死亡是近几年国自然热点之一,铁死亡与铁质相关,与细胞凋亡、细胞坏死、细胞自噬等不同,是一种新的细胞程序性死亡方式。
铁死亡是由铁积累和脂质过氧化驱动的一种RCD形式,其特征在于线粒体变小、线粒体嵴减少、线粒体膜密度增加以及线粒体膜破裂增加。
铁死亡的主要机制是在二价铁或酯氧合酶的作用下,催化细胞膜上高表达的不饱和脂肪酸,发生脂质过氧化,从而导致细胞死亡并伴随抗氧化体系(GSH系统)调节核心酶GPX4的降低。
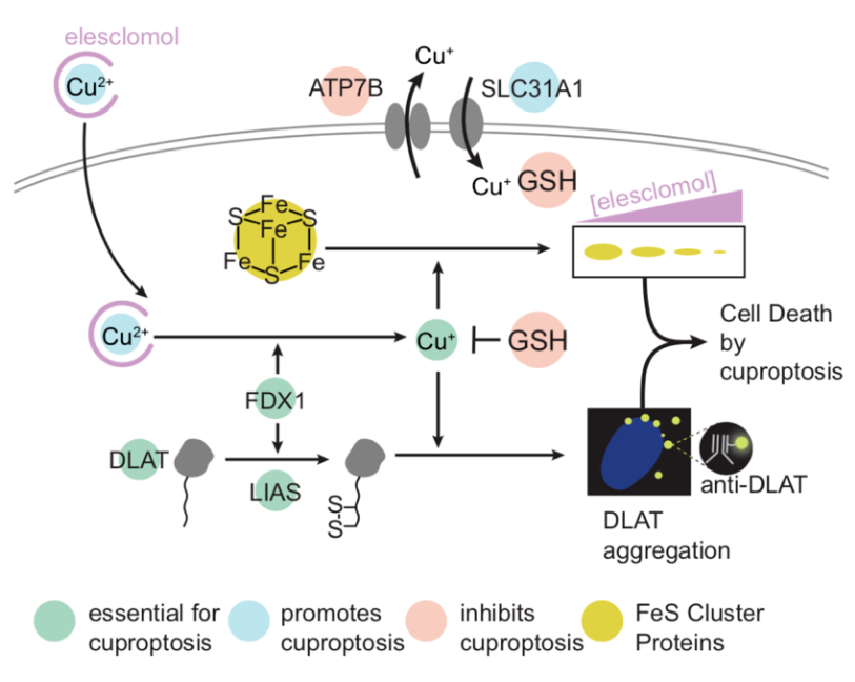
06 铜死亡
铜死亡的潜在机制为通过铜离子与TCA中硫辛酰化蛋白的结合,促使硫辛酰化蛋白发生异常寡聚化,此外,铜离子还可降低Fe-S簇蛋白水平,二者共同诱发蛋白质毒性应激反应最终导致细胞死亡。
07 溶酶体依赖性细胞死亡
溶酶体依赖性细胞死亡(LCD),也称为溶酶体细胞死亡,是由LMP释放的水解酶(组织蛋白酶)或铁来介导的一种RCD形式,其特征是溶酶体破裂。
当细胞暴露于溶酶体洗涤剂、二肽甲酯、脂质代谢物和ROS时,溶酶体破裂,继而释放大量的水解酶,导致LCD的发生。
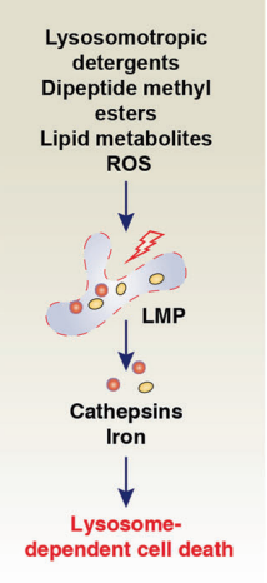
其中组织蛋白酶在LCD中起主要作用,阻断组织蛋白酶的表达或活性可减轻LCD的发生。溶酶体膜透化还可以在细胞凋亡、自噬依赖性细胞死亡和铁死亡的过程中放大细胞死亡信号传导,从而增加细胞死亡途径的复杂性。
08 Parthanatos
Parthanatos是一种PARP1依赖性RCD形式,由氧化应激诱导的DNA损伤激活,它可以分为两种类型:
AIFM1依赖型Parthanatos:活化的PARP1结合AIFM1,介导AIFM1从线粒体移位到细胞核,继而导致部分染色体的溶解。
AIFM1非依赖型Parthanatos:在某些条件下可发生,如干性黄斑变性。
AIFM1依赖性和非依赖性Parthanatos与其他RCD(如自噬依赖性细胞死亡和坏死性凋亡)之间的相互影响可能涉及DNA损伤相关的疾病,如神经退行性疾病,心肌梗塞和糖尿病。
09 Oxeiptosis
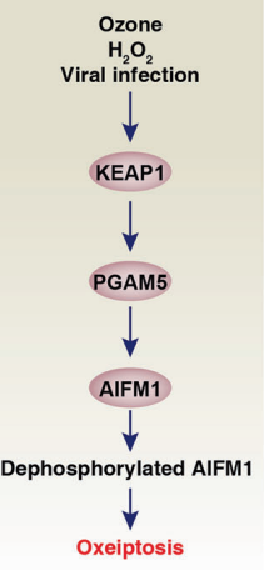
Oxeiptosis是氧自由基诱导的不依赖半胱天冬酶的新型RCD,这一过程由KEAP1-PGAM5-AIFM1途径驱动。
过度活化的KEAP1能以NFE2L2非依赖性方式介导H2O2诱导的Oxeiptosis,通过KEAP1-PGAM5途径介导AIFM1 Ser116的去磷酸化。
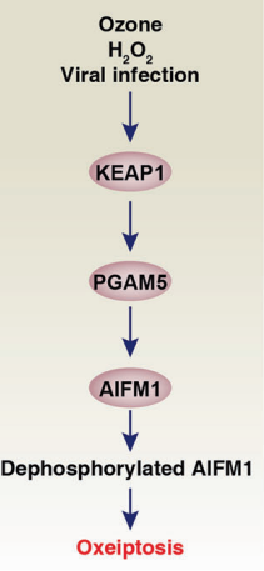
现有研究并未揭示Oxeiptosis在人类疾病中的作用。
10 细胞入侵性死亡
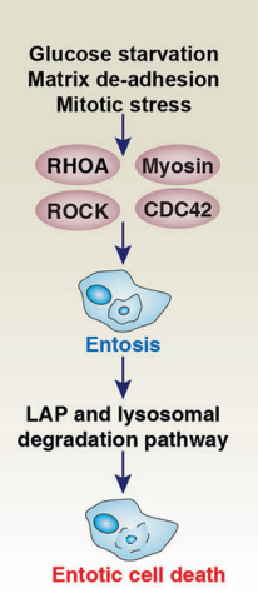
细胞入侵性死亡(Entotic cell death)是细胞“同类相食”的一种RCD形式,简单来说,就是一个细胞吞噬并杀死另一个细胞,它的特征是细胞内细胞结构。
细胞入侵性死亡激活后,通过LC3相关的吞噬作用(LAP)和组织蛋白酶B(CTSB)介导的溶酶体降解途径吞噬和杀死同类细胞。
这一细胞死亡过程中的调控包括两种:
细胞粘附和细胞骨架重排通路(如肌动蛋白、肌球蛋白、RHOA和ROCK)在控制Entosis诱导作用中起重要作用。
信号分子和调节因子(如CDC42)也通过不同的机制参与Entosis的调节。
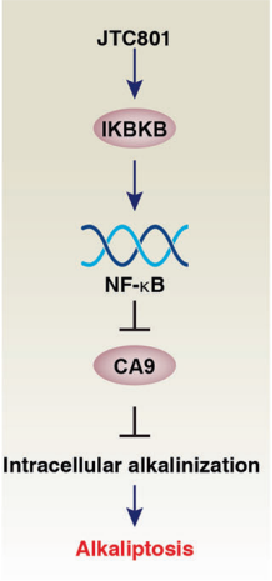
11 碱死亡
碱死亡(Alkaliptosis)是一种由细胞内碱化作用驱动的新型RCD。关于其过程,目前可以了解到IKBKB-NF-κB途径依赖性碳酸酐酶9(CA9)的下调可以诱导Alkaliptosis的发生,但其具体分子作用机制仍不清楚。
12 Netotic cell death
Netotic cell death(NETosis)是由NET驱动的一种RCD形式,其受NADPH氧化酶介导的ROS产生和组蛋白瓜氨酸化的调节。
NETosis是涉及多个信号和步骤的动态过程,这一过程包括四个环节,分别是NADPH氧化酶介导的ROS产生、细胞自噬、颗粒酶的释放和转运,以及Cathelecidin家族多肽从细胞质到细胞核的易位。
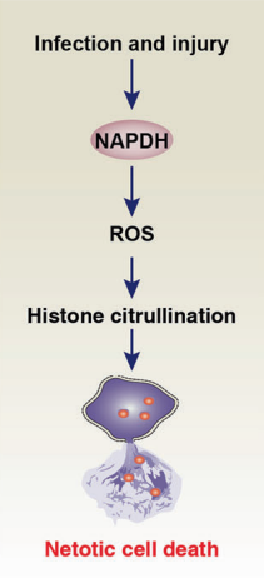
NETosis介导组蛋白瓜氨酸化,最终导致染色质去浓缩、核膜破坏和染色质纤维的释放。
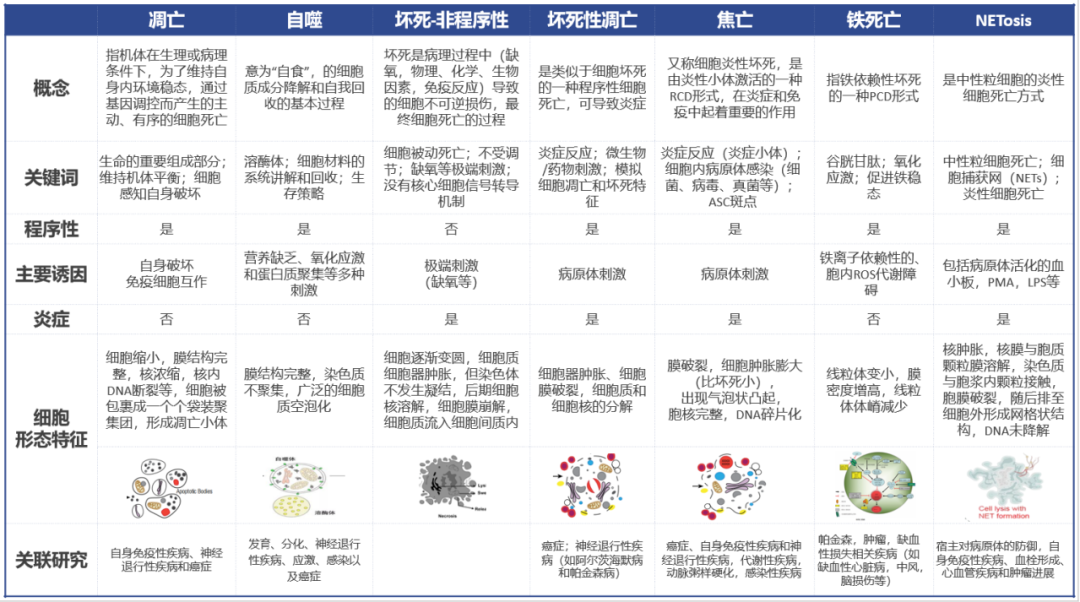
五、总结
下表总结对比了部分典型的细胞死亡方式。
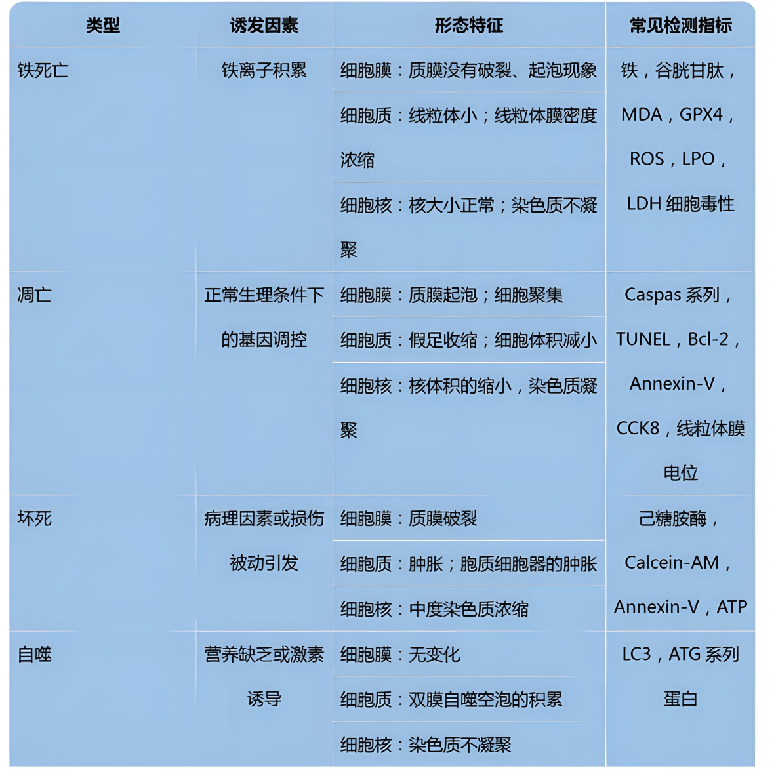
针对比较热门的铁死亡、凋亡、坏死和自噬,我们另外总结了它们的诱发因素、形态特征以及常见检测指标。
 文章推荐
文章推荐