
黄疸是指由于高胆红素血症所引起的皮肤和黏膜的黄色改变。那么关于黄疸有什么课题设计思路呢?今天我们一起来探讨一下。
下面,我们将分享一篇发表于中科院1区期刊SCIENCE TRANSLATIONAL MEDICINE,影响因子为15.8的高分文献,名为《胆红素增强ASIC通道活性,加重新生儿高胆红素血症小鼠的神经毒性》,希望能给大家带来不一样的灵感~

【文章题目】:胆红素增强ASIC通道活性,加重新生儿高胆红素血症小鼠的神经毒性
【发表期刊】:SCIENCE TRANSLATIONAL MEDICINE
【影响因子】:IF=15.8
【发表日期】:2020.02
一、研究背景
①新生儿高胆红素血症,即血清胆红素浓度升高,已知会损害神经功能和形态。
②缺血和缺氧引起的酸化可以直接激活酸感离子通道(ASIC),ASIC是变性素/上皮钠通道超家族的成员。
③这些通道形成ASIC亚基的同源异源三聚体:1a、1b、2a、2b、3和4,其中ASIC1a、2a和2b是在中枢神经系统中发现的主要亚基。
④目前的概念范式认为酸中毒可以增强新生儿大脑中胆红素的过载,但胆红素与ASIC依赖性神经毒性之间的相互关系仍然未知。
二、技术路线
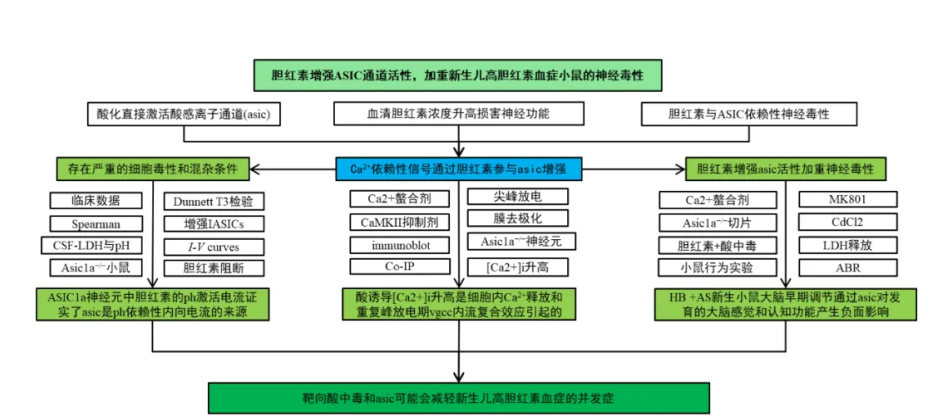
三、研究结果
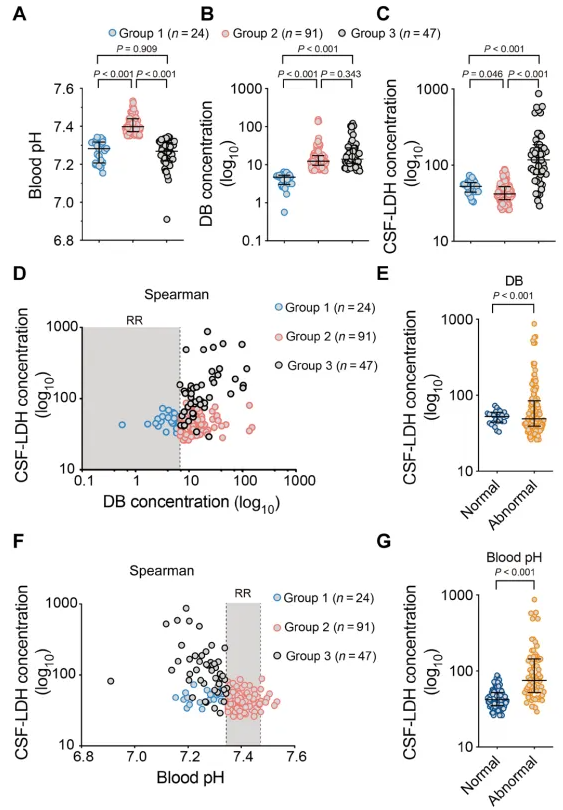
1.血胆红素和pH值与高胆红素血症和/或酸中毒婴儿脑脊液(LDH)的交叉相关分析
为了定量研究血液胆红素浓度、pH与细胞损伤/死亡之间的关系,作者收集了162例高胆红素血症和/或酸中毒婴儿的数据,如图1A~C,Dunnett T3检验提示存在严重的细胞毒性和混杂条件。图1D显示,LDH中的乳酸脱氢酶(CSF-LDH)与直接胆红素(DB)浓度或pH的变化没有很强的相关性,但当发生并发酸中毒时,与DB浓度在很宽的浓度范围内高度相关。图1F显示,伴有高胆红素血症的3组新生儿CSF-LDH与血液pH值的轻微下降密切相关。CSF-LDH也与酸中毒相关,但与高胆红素血症无关。此外,我们可以从图1E、1G结果观察到,血pH异常新生儿CSF-LDH平均浓度高于血pH正常新生儿。这些结果表明:假设胆红素本身具有有限的毒性,那么可能加剧酸中毒依赖性神经元损伤。
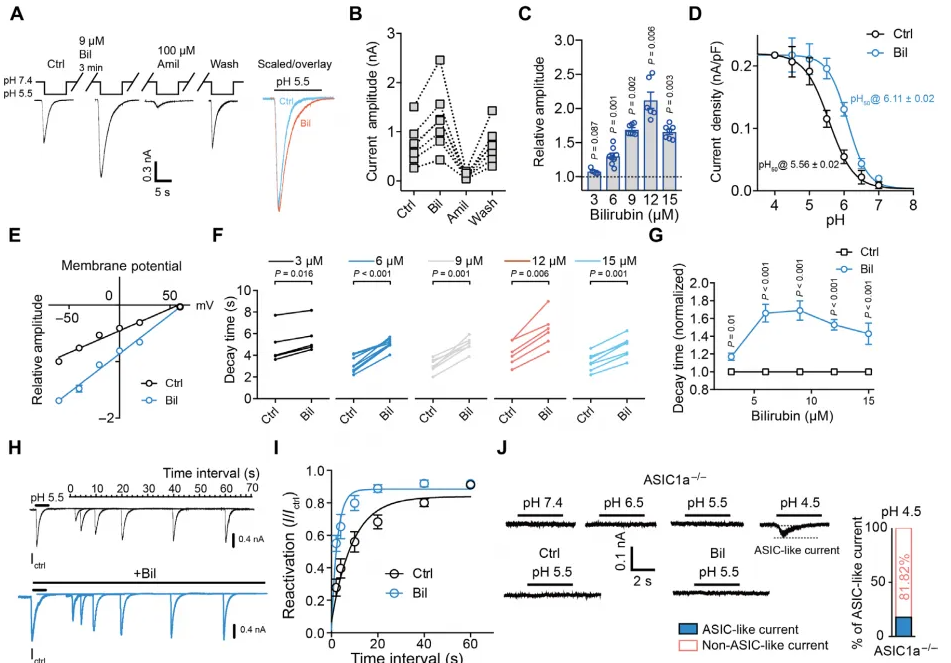
2.胆红素以pH依赖性和电压依赖性的方式增强ASIC电流
为了测试IASICs是否以及如何被胆红素调节,作者将前庭内侧核(MVN)神经元暴露于浓度低于LDH游离胆红素平均值的胆红素中,使用基于unagi荧光蛋白(UnaG)的检测方法直接测量,图2A~B显示,在反复呈现酸的情况下,IASICs在应用胆红素后3分钟内增强,在胆红素完全清除后,这种作用是可逆的。接着,向MVN神经元提供了一系列持续3分钟的胆红素,如图2C所示,发现在12µM时达到最大增强。我们还可以从图2C~D发现,在较低的pH值下,胆红素比在较高的pH值下产生相对更大的IASICs,导致pH剂量-反应曲线明显偏移。我们从图2E发现,这种IASICs的增强似乎与ASIC的膜电位或通透性无关,因为胆红素在−60~+60mV的所有电位范围内对IASICs的增强程度相似,而逆转电位保持不变。总的来说,这些发现表明胆红素使ASIC对质子更敏感,并增强了它们的弦传导,这是MVN神经元中ASIC振幅增加的原因。图2F~I进一步的实验表明,胆红素减缓了ASIC的脱敏并加速他们从脱敏中恢复,再次表明其对MVN神经元ASIC门控的作用。图2J显示,在ASIC1a神经元中胆红素的pH激活电流记录独立证实了ASIC是pH依赖性内向电流的来源。
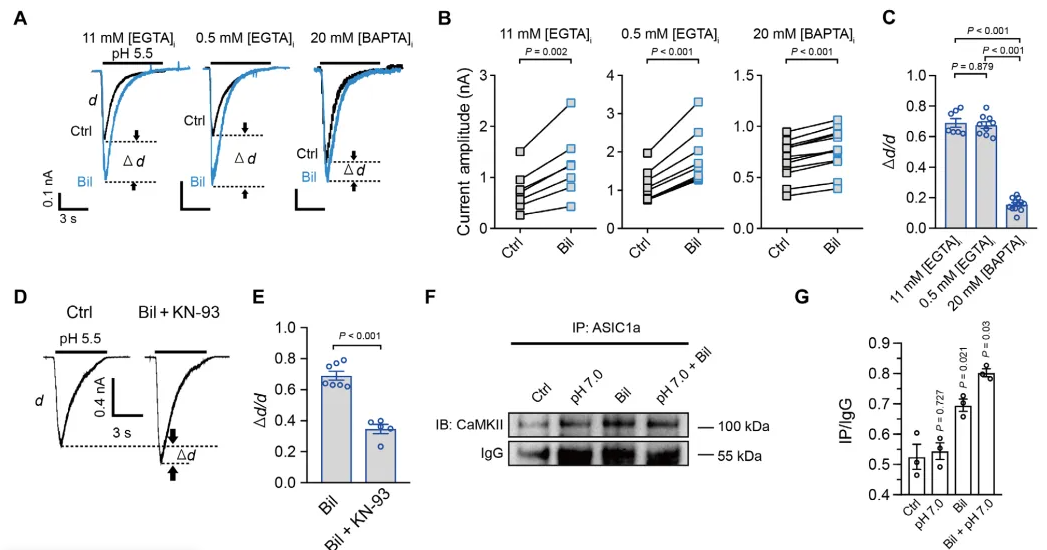
3.Ca2+依赖性信号通过胆红素参与ASIC的增强
鉴于胆红素可以很容易地渗透细胞膜,并通过细胞内Ca2+([Ca2+]i)依赖的途径调节神经元活动,作者研究了胆红素是否需要[Ca2+]i来增强IASICs。我们可以从图3A看到,作者测试了两种Ca2+螯合剂EGTA和BAPTA的效果。图3B~C显示,20mM BAPTA在细胞内螯合[Ca2+]i可减弱胆红素诱导的IASICs增强,而11mM EGTA则没有效果。BAPTA对胆红素增强IASICs的阻断作用提示其参与了Ca2+依赖的细胞内信号通路,如蛋白激酶。为此,我们可以从图3D看到作者测试了钙-钙调蛋白依赖性蛋白激酶II(CaMKII)的抑制剂。图3E显示,添加5µM KN-93减弱了IASICs的增强。接着,作者利用抗CaMKII和ASIC1a抗体的免疫沉淀和免疫印迹分析,如图3F~G所示,发现在孵育1小时后,胆红素增加了ASIC1a下拉中CaMKII特异性条带的强度,表明胆红素促进了ASIC1a和CaMKII之间的关联。这些结果表明,CaMKII依赖性ASIC(或其附属蛋白)的磷酸化可能是MVN神经元中胆红素对ASIC的Ca2+依赖性上调的原因。
4.胆红素和酸对神经元兴奋性产生协同作用
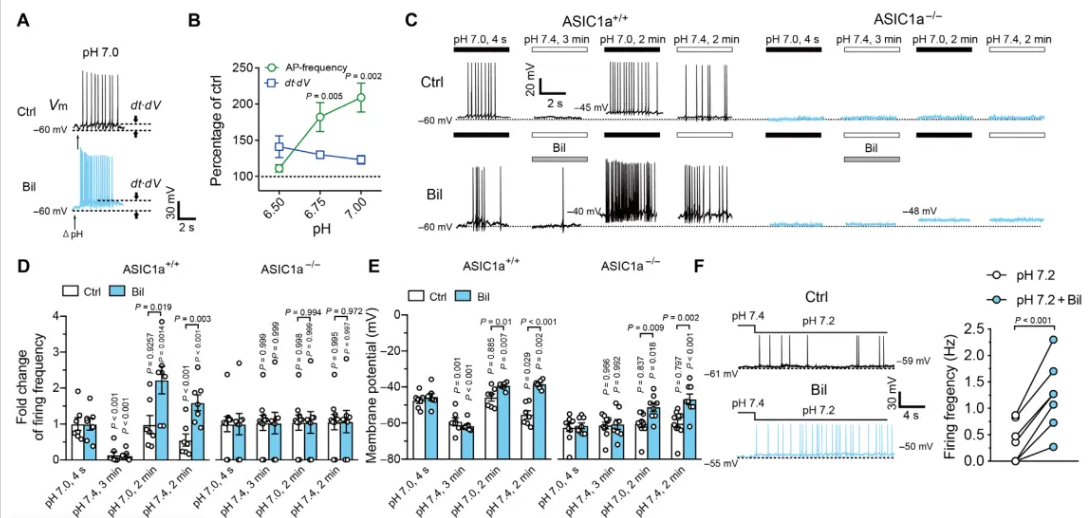
为了直接测试IASICs胆红素依赖性增强对神经元兴奋性的功能影响,作者进行了电流钳记录,以检测胆红素暴露时ASIC激活对MVN神经元的影响。图4A~B显示,酸碱值从7.4到6.5~7.0,胆红素被发现增加发射频率,但适度降低至pH7.0,似乎产生了最大的增强,而酸化程度更高的溶液会导致去极化阻止尖峰。相比之下,我们可以从图4C看到,细胞外pH7.0溶液灌注2分钟后,即使切换回pH7.4溶液,也会引起持续的膜去极化和持续的尖峰放电,这表明MVN神经元兴奋性的增加可能是持久的。虽然单独胆红素不产生膜去极化,但在暴露于pH7.0溶液2分钟期间和之后,胆红素显著提高了放电速率。相反,图4C~D显示,在Asic1a−/−神经元中没有观察到这种变化。图4E显示,在切换回pH值7.4后,野生型和Asic1a−/−神经元都出现了轻微但持续的去极化,随后出现了胆红素。这些结果表明,胆红素可以增强酸依赖性神经元的兴奋性和放电,协同促进病理性酸中毒和高胆红素血症期间的神经元过度兴奋。
5.胆红素增强酸诱发的细胞内Ca2+瞬态
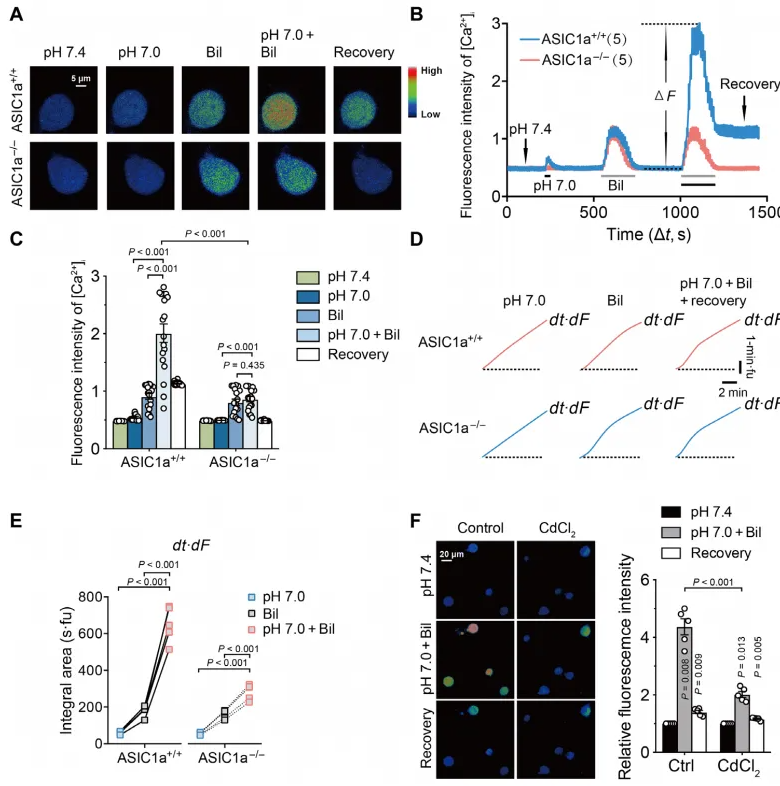
在美国,胆红素本身可以通过短暂的灌注引起小的[Ca2+]i升高。同理,如图5A所示,胆红素暴露增强了WT MVN神经元中酸诱导的[Ca2+]i升高,而这种作用在Asic1a−/−细胞中被阻断。图5B~C显示,在pH7.4溶液中长时间冲洗后,WT神经元中[Ca2+]i的荧光强度保持在比Asic1a−/−神经元更高的浓度。图5D~E对Ca2+反应的积分区域的比较表明,胆红素对酸诱导的[Ca2+]i升高的影响是ASIC依赖性的、持久的、超线性的。这一结果表明胆红素延长ASIC的开放以增加神经元的兴奋性,导致[Ca2+]i过载,从而导致神经毒性。已知低pH诱发的动作电位促进电压依赖性钙通道(VGCC)的活性,这可能导致Ca2+的过量流入。图5F显示,在溶液中加入CdCl2,可以减弱[Ca2+]i的升高,这表明酸诱导的[Ca2+]i升高主要是由细胞内Ca2+释放和在重复峰放电期间通过VGCC内流的复合效应引起的。
6.胆红素通过增强ASIC的活性而加重神经毒性作用
为了直接测试胆红素是否通过ASIC加重细胞死亡,作者又通过活细胞和死细胞对WT和Asic1a−/−小鼠的荧光染色进行细胞损伤试验。图6A显示,在胆红素存在的情况下,酸化增强了WT中的神经死亡,但在Asic1a−/−切片中没有。图6B显示,钙离子螯合剂也降低了MVN神经元的死亡率。我们可以从图6C发现,在胆红素和酸条件下,MK801降低了WT的死亡率,但在Asic1a−/−神经元中却没有,这意味着在高胆红素血症和酸中毒条件下,ASIC在介导细胞死亡方面起主导作用。图6D显示,CdCl2在减轻细胞死亡方面最有效,与前面结果一致。同样,我们可以从图6E看到,在pH7.0时,胆红素增加了ASIC1a/2a-GFP转染的CHO细胞的死亡率(P<0.001)。这些数据有力地证明,含有ASIC1a的通道是细胞内Ca2+超载后胆红素诱导的细胞死亡的分子底物。
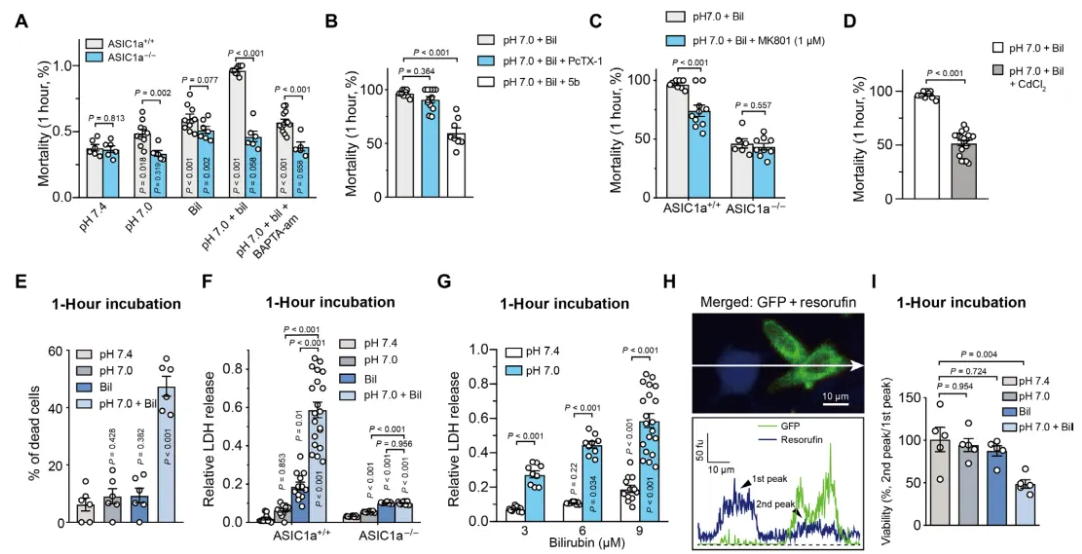
接着,我们可以从图6F~G观察到,胆红素对增强Asic1a−/−神经元的细胞损伤是无效的并对LDH释放的影响呈浓度依赖性。图6H~I显示,胆红素和pH7.0的共同应用导致CHO细胞的降低,这表明胆红素本身对细胞活力有微妙的影响,但通过含有ASIC1a的通道加重了细胞损伤。这些结果支持高胆红素血症与酸中毒介导的细胞损伤和死亡之间的新的功能联系。
7.小鼠新生儿并发高胆红素血症和酸中毒对脑功能造成长期损害
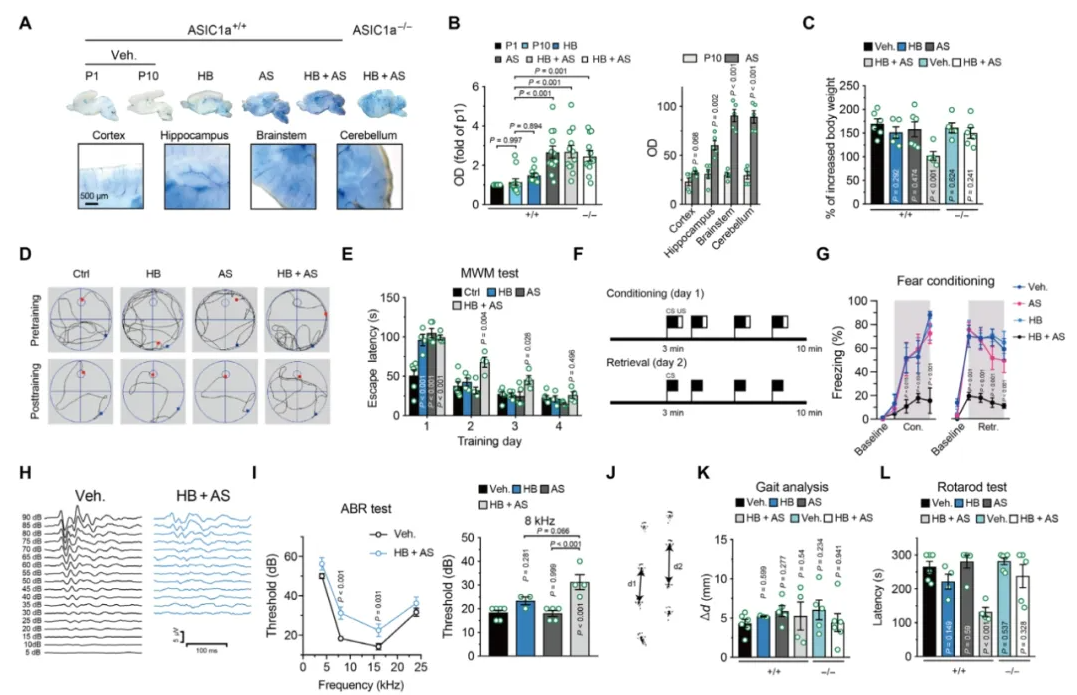
为了模拟体内高胆红素血症伴或不伴酸中毒的影响,作者将新生小鼠置于三种单独的实验条件下,持续1周。图7A~B显示,AS组和AS+HB组的脑切片全部被染成蓝色,尤其是海马、脑干和小脑,皮质染色极少。这些结果表明,是酸中毒而不是高胆红素血症增加了血脑屏障的通透性,并且这种作用不依赖于ASIC。图7C显示,HB+AS小鼠的体重增加是最低的,暗示同时发生的高胆红素血症和酸中毒对发育的整体负面影响。图7D~G的一系列行为实验表明HB+AS组新生小鼠早期阶段的条件反射可导致后来显著的空间学习和记忆异常。通过测量和比较听觉脑干反应,我们可以从图7H~I发现HB+AS WT小鼠在所有频率下都表现出阈值向上移动。我们还可以从图7J~L发现,当用加速旋转杆刺激这些小鼠时,HB+AS WT小鼠表现出停留在杆上的缺陷,这可以从下降潜伏期减少50%得到证明。这种缺陷在Asic1a−/−小鼠中完全不存在。以上结果表明,HB+AS新生小鼠大脑的早期调节可以通过ASIC对发育中的大脑的感觉和认知功能的长期轨迹产生负面影响。
四、研究小结
通过本研究,作者发现在患有高胆红素血症和酸中毒的婴儿中,CSF中细胞死亡标志物LDH的浓度会升高,并且与酸中毒的严重程度而不是胆红素浓度的升高有更强的相关性。在小鼠新生儿神经元中,胆红素表现出有限的毒性,但会增强ASIC的活性,导致细胞内Ca2+浓度升高、尖峰跃动和细胞死亡。此外,新生儿同时接受高胆红素血症和缺氧诱导的酸中毒调理,会促进体内学习和记忆以及复杂感觉运动功能的长期损伤。这些损伤在ASIC1a缺失的小鼠中基本减轻。这些发现表明,针对酸中毒和ASIC可减轻新生儿高胆红素血症并发症。
五、国自然中标情况

 文章推荐
文章推荐