
细胞自噬,简单的说,就是细胞“自己吃自己”,是真核生物中进化保守的对细胞内物质进行周转的重要过程。那么关于细胞自噬有什么课题设计思路呢?今天我们一起来探讨一下。
今天我们将分享一篇发表于中科院1区期刊Autophagy,影响因子为14.6的文献,希望能给大家带来不一样的灵感。
一、课题挂靠与SCI信息

【文章题目】:儿茶素EGCG促进FTO降解保护胰腺β细胞免受过度自噬诱导的损伤以防治糖尿病
【发表期刊】:Autophagy
【影响因子】:14.6/中科院1区
【课题挂靠】:①国家自然科学基金[82330027];②国家自然科学基金[82170810];③国家自然科学基金[82370803]
二、研究背景
①EGCG是绿茶中最主要的活性儿茶素,在胰腺胰岛和β细胞保护方面表现出广泛的功能特性;
②在自噬过度活跃的BECN1F121A小鼠中,由于胰岛素颗粒过度降解,自噬过度诱导会降低胰岛素分泌和胰岛素储存;
③前期发现糖皮质激素受体(NR3C1)/FTO轴介导过度自噬诱发β细胞功能障碍;
三、技术路线
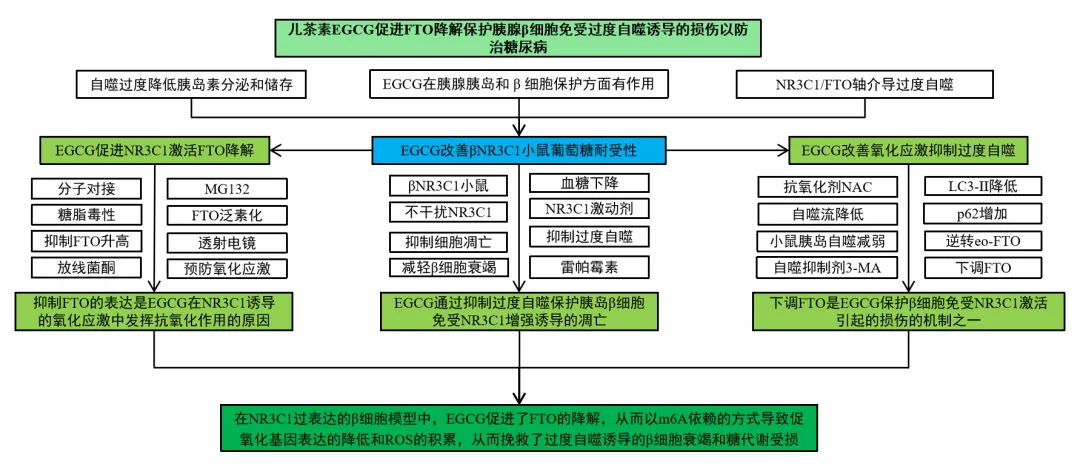
四、研究结果
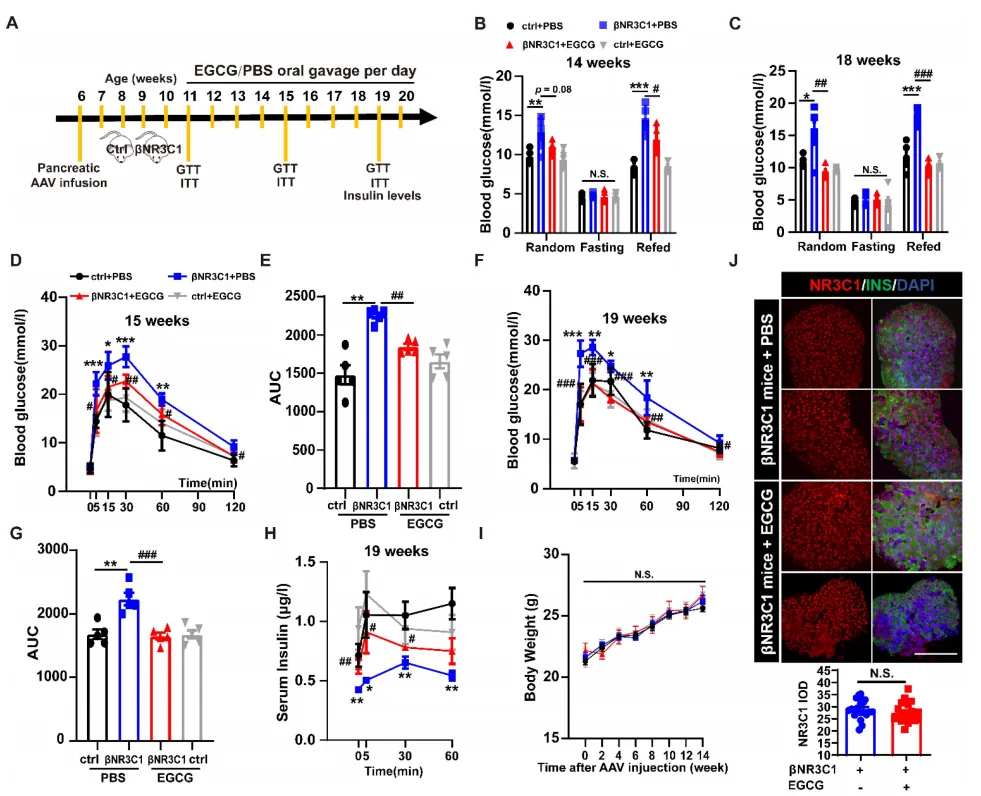
1.EGCG可改善β细胞特异性NR3C1过表达小鼠的葡萄糖耐受性和β细胞功能
为深入探究EGCG的作用,作者在图1A中构建了β细胞特异性NR3C1过表达(βNR3C1)小鼠模型。图1B~H显示,EGCG给药后,βNR3C1小鼠的糖尿病相关表型逐渐改善,表现为14周龄和18周龄的血糖下降,15周龄和19周龄的葡萄糖耐受不良减轻,胰岛素分泌水平显示显著反弹。值得注意的是,图1J显示EGCG并没有干扰β细胞中NR3C1的过表达。图1K~M显示,体外胰岛灌注实验表明NR3C1过度激活显著抑制高葡萄糖偶联胰岛素分泌,被EGCG口服逆转;此外,口服EGCG也有效地保护了β细胞免受NR3C1诱导的凋亡。总之,EGCG对NR3C1过度激活诱导的β细胞衰竭和糖尿病具有保护作用。
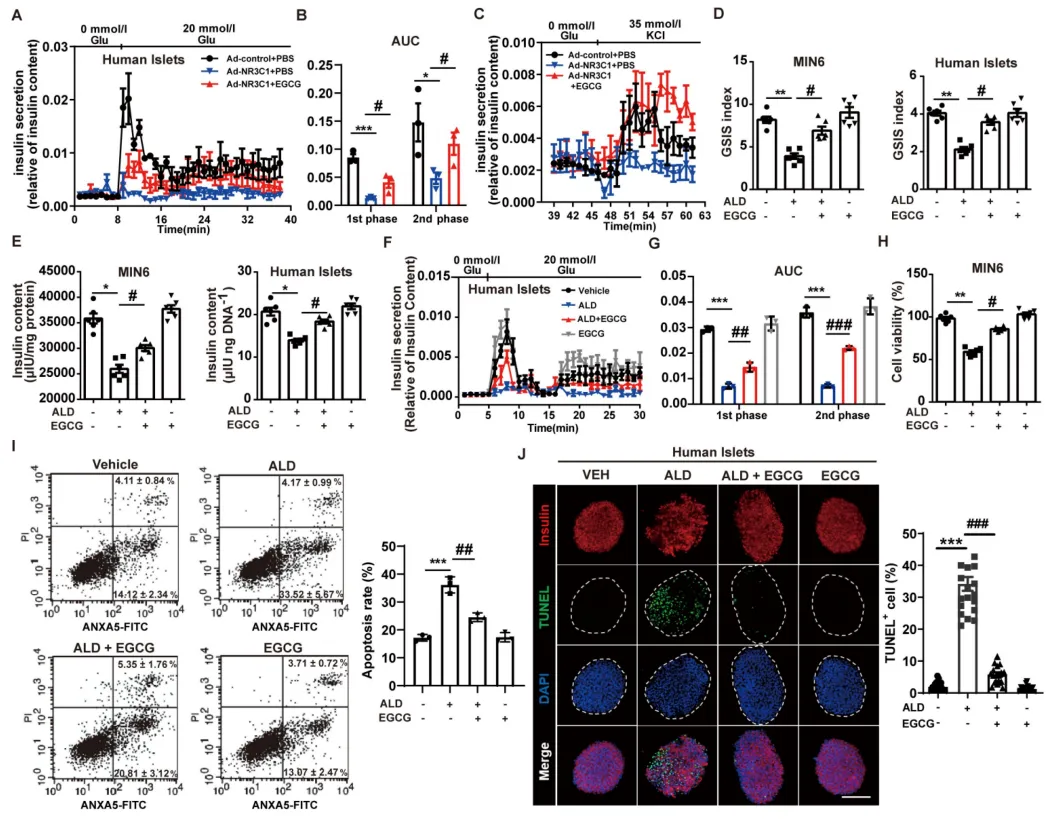
2.EGCG逆转NR3C1激活诱导的胰腺β细胞衰竭
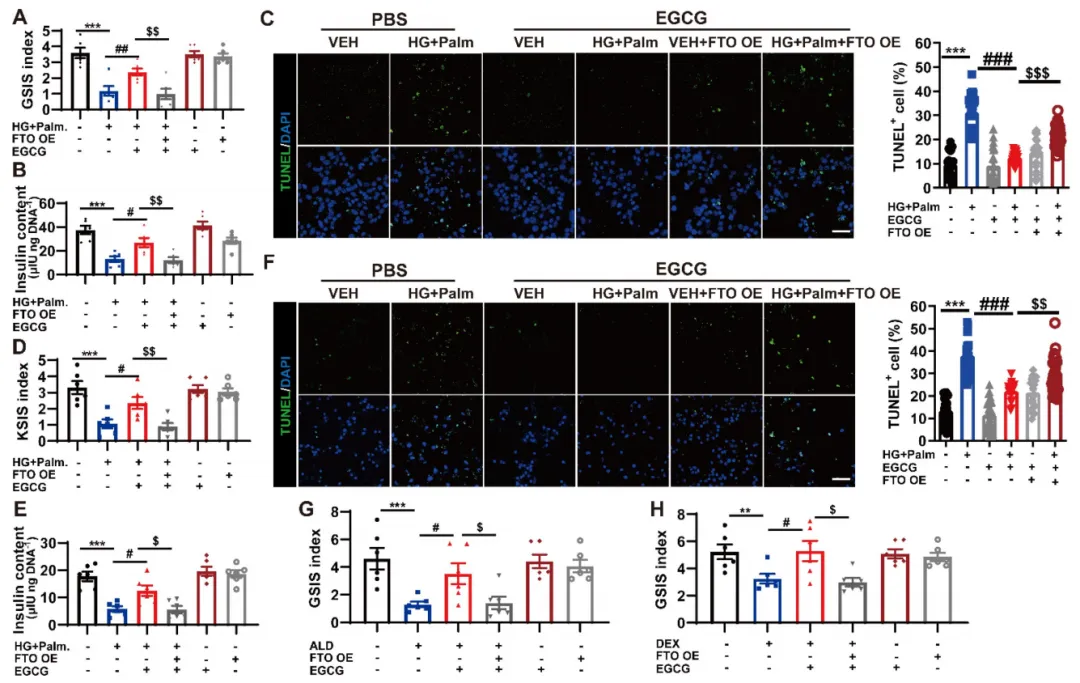
为了更全面且深入地验证EGCG的作用机制,研究人员开展了体外实验,选用人胰岛和MIN6细胞作为研究对象。图2A~C的灌注分析表明,EGCG可有效改善过表达NR3C1的人胰岛的胰岛素分泌情况。在利用醛固酮(ALD)或地塞米松(DEX)诱导NR3C1过激活后,图2D ~E实验发现EGCG能够显著恢复β细胞因ALD或DEX处理而受损的胰岛素分泌和胰岛素含量。对于孤立的人胰岛在胰岛灌注过程中受ALD处理后的胰岛素分泌情况,如图2F ~G所示,EGCG也可实现部分逆转。此外,图2H显示EGCG还可以改善ALD或DEX处理的MIN6细胞的活力下降。图2I~J的流式细胞术和TUNEL检测进一步证明,EGCG减少了ALD处理的MIN6细胞和人胰岛中的β细胞凋亡。这些结果表明,EGCG减轻了NR3C1过度激活引起的β细胞衰竭。
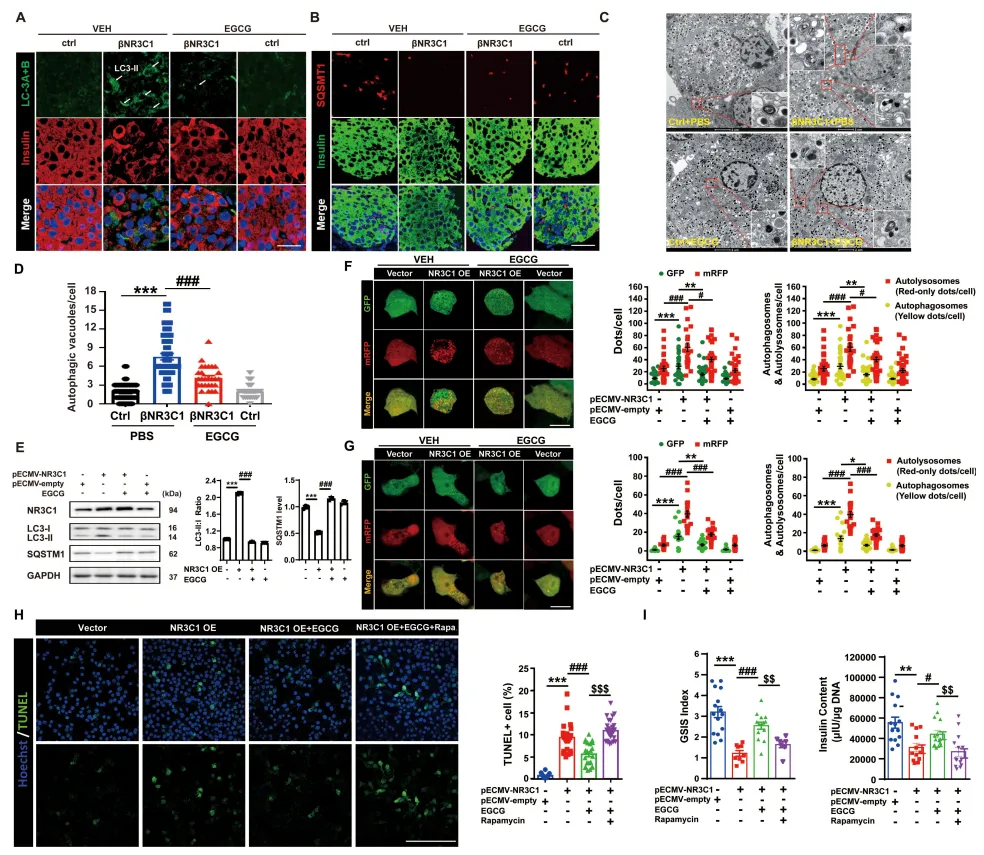
3.EGCG通过抑制过度自噬保护胰岛β细胞免受NR3C1诱导的凋亡
鉴于已有研究表明过度自噬参与了NR3C1增强诱导的胰腺β细胞功能障碍和凋亡,研究人员进而深入探究EGCG是否通过调节自噬发挥其保护作用。在βNR3C1小鼠中,如图3A~B所示,NR3C1过表达增加了胰腺中MAP1、LC3I/lc3II阳性和SQSTM1/p62阴性细胞的数量,而EGCG的使用减弱了这些变化。此外,图3C~D中,βNR3C1小鼠β细胞的透射电子显微镜(TEM)图像显示自噬空泡聚集,EGCG给药后明显减轻。因此,NR3C1过表达导致LC3-II表达增加,但SQSTM1蛋白水平降低,这一情况在图3E中发现被EGCG部分逆转。图3F~J显示,mRFP-GFP-LC3的免疫荧光染色也证实,在MIN6和INS1细胞中,EGCG抑制NR3C1增强诱导的自噬的过度激活;EGCG对NR3C1刺激的细胞凋亡增加和胰岛素分泌受损的保护作用在自噬激活剂处理的人胰岛和MIN6细胞中被消除。总之,EGCG通过抑制过度自噬保护胰岛β细胞免受NR3C1增强诱导的凋亡。
4.EGCG促进NR3C1增强激活的β细胞FTO降解
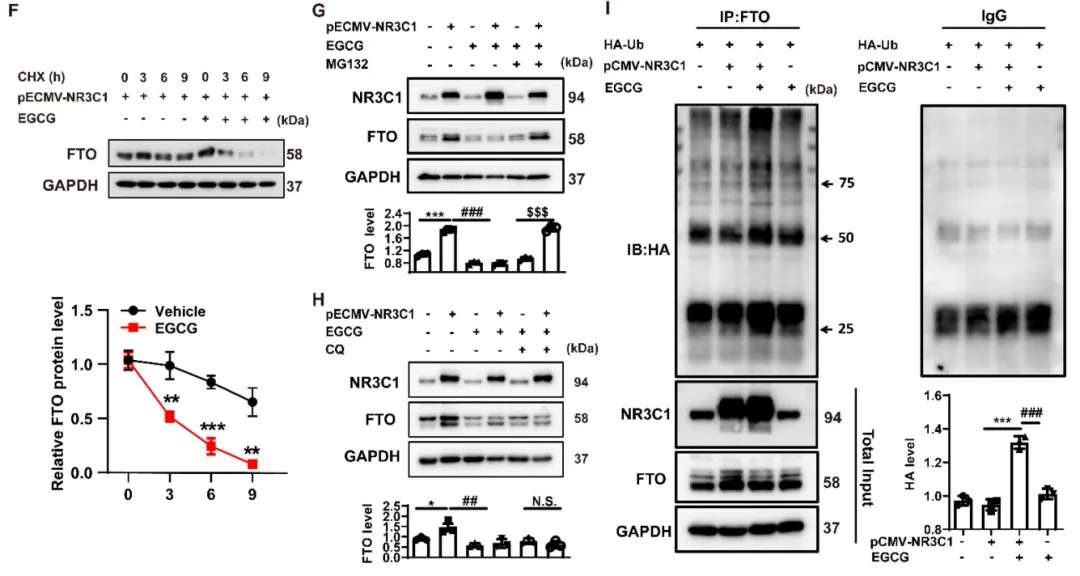
据报道,EGCG可抑制FTO的表达,而FTO可导致NR3C1增强诱导的β细胞过度自噬和功能障碍。图4A中他们利用分子对接研究了FTO和EGCG之间的相互作用,对接评分为-9.0 kcal/mol, EGCG与FTO蛋白形成紧密结合。图4B显示,EGCG可以阻止慢性高糖和棕榈酸引起的β细胞FTO表达的增加,而对NR3C1表达的增加没有影响。图4C显示,2型糖尿病(T2D)受试者的胰岛处理导致β细胞中FTO表达被EGCG降低。此外,从图4D~E可看出,EGCG在体内外均抑制了NR3C1过表达β细胞中FTO蛋白水平的升高。图4F~I显示,应用蛋白质合成抑制剂CHX,发现EGCG显著促进过表达NR3C1的MIN6细胞中FTO的降解;当蛋白酶体被MG132抑制时,EGCG对FTO降解的作用被消除;相反,溶酶体抑制剂氯喹(CQ)没有影响;在NR3C1过表达的情况下,EGCG刺激了FTO泛素化。综上,EGCG在翻译后水平减弱NR3C1诱导的FTO表达。
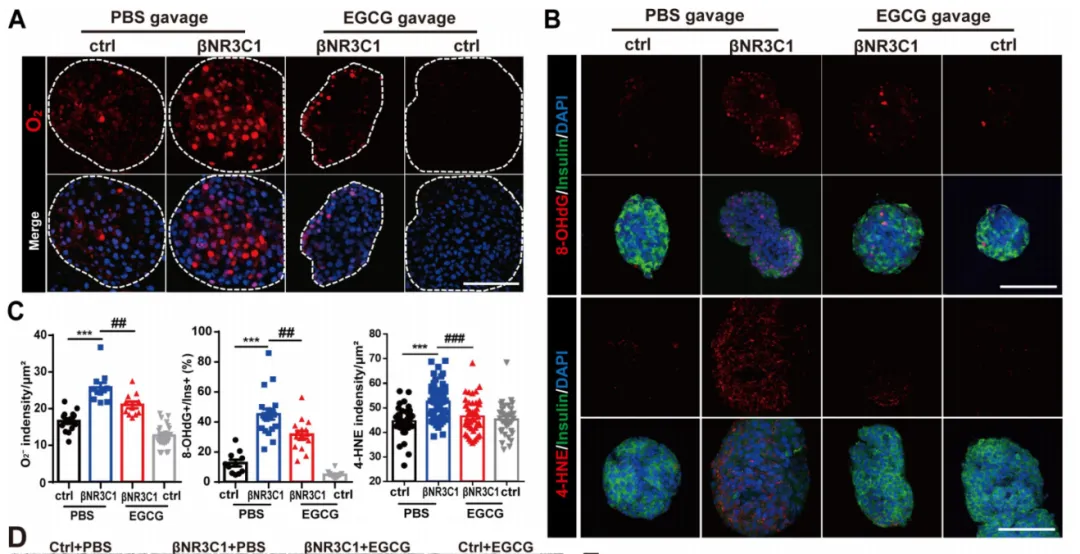
5.EGCG通过抑制FTO的表达抑制NR3C1诱导的氧化应激
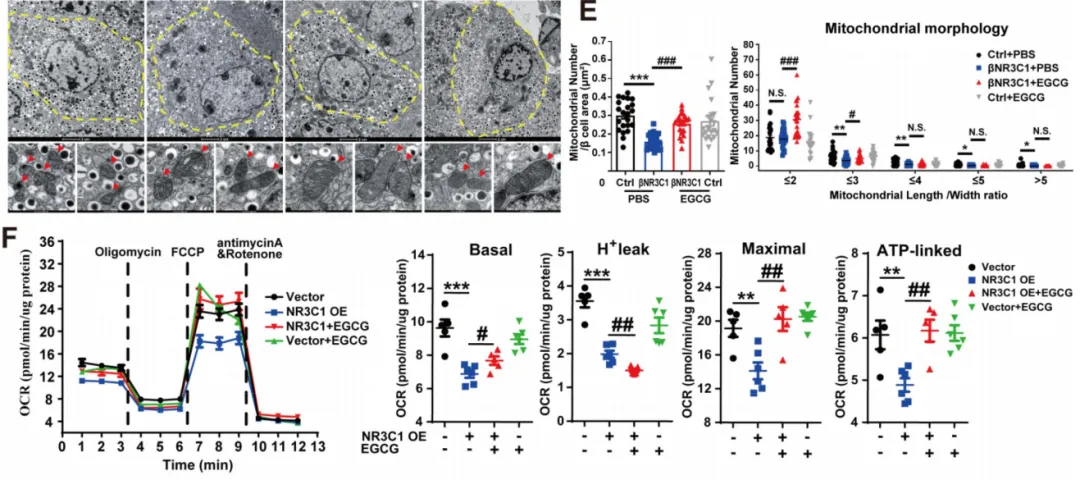
鉴于EGCG具有抗氧化特性,研究人员深入探究了其与氧化应激之间的关联。在βNR3C1小鼠中,如图5A~C所示,NR3C1过表达导致O2、4-HNE和8-OHdG显著增加,可被EGCG逆转。在图5D~E的透射电镜结果图观察到,βNR3C1小鼠的β细胞出现明显的线粒体损伤,线粒体数量明显减少,在EGCG治疗后可以显著改善。图5F的β细胞线粒体氧化磷酸化结果表明,βNR3C1小鼠胰岛的基础呼吸、ATP生成和最大呼吸能力受损,EGCG处理可以改善这一情况。图5G显示,来自βNR3C1小鼠的胰岛显示出复合物I和复合物III的蛋白水平明显降低,这一水平在EGCG进一步处理后减弱。此外,如图5H所示,EGCG可降低过表达NR3C1的MIN6细胞产生和NO释放。这些数据表明,EGCG对NR3C1诱导的线粒体功能障碍具有保护作用,可以预防NR3C1增强诱导的氧化应激。
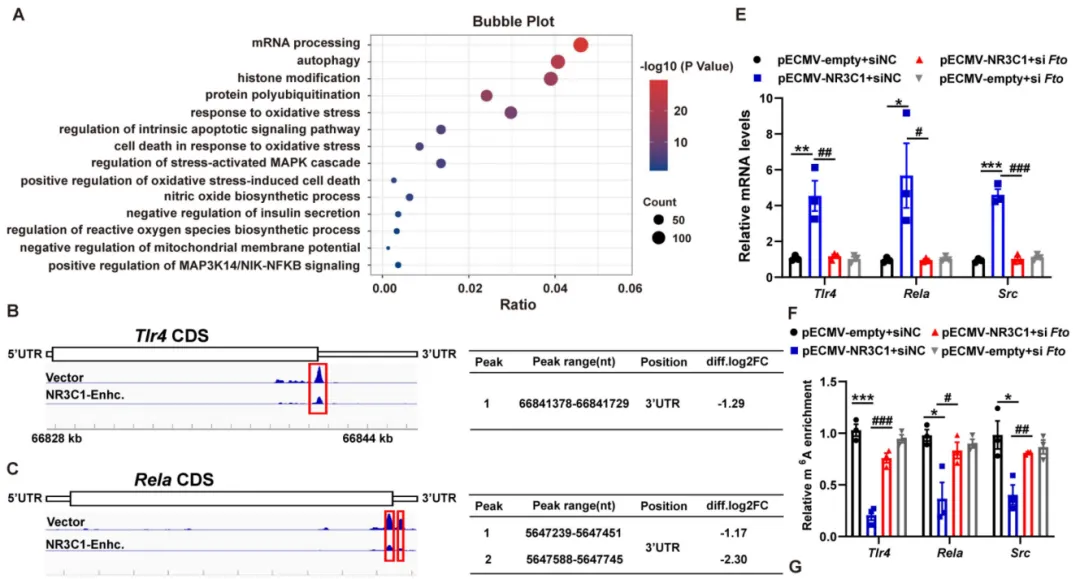
结合图6A~D转录组信息,他们发现Tlr4、Rela和Src可能在FTO调控NR3C1诱导的氧化应激中发挥重要作用。图6E~I显示,FTO敲低显著消除了NR3C1过表达MIN6细胞中Tlr4、Rela和Src的上调,同时消除了NR3C1增强引起的这些转录本上m6A水平的下降;EGCG防止了过度的Tlr4、Rela和Src水平,增加了过表达NR3C1的MIN6细胞产生和NO释放,这可以被FTO过表达所抑制。这些结果证实了抑制FTO的表达是EGCG在NR3C1诱导的氧化应激中发挥抗氧化作用的原因。
6.EGCG通过改善氧化应激抑制FTO诱导的过度自噬
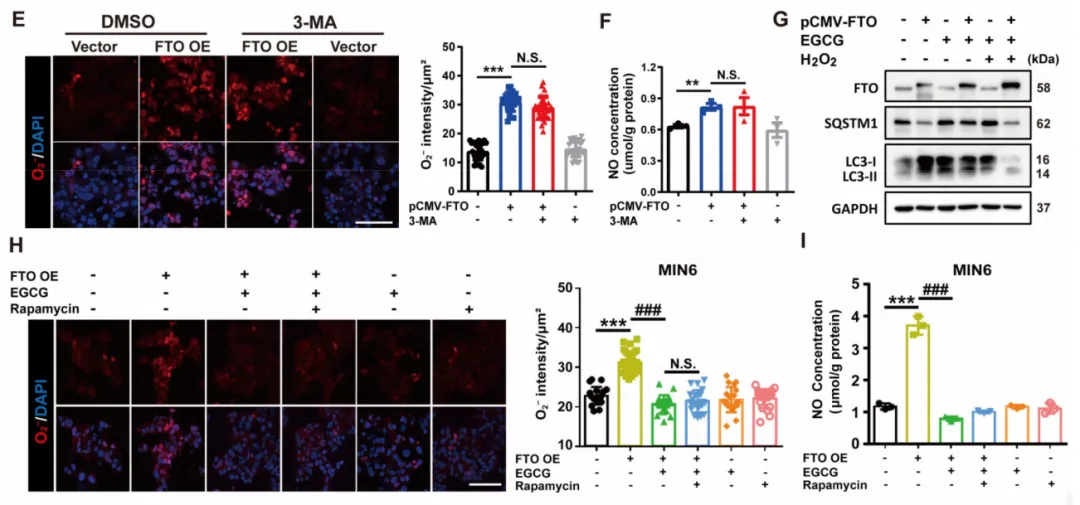
五、研究小结
本研究探讨了EGCG对体内β细胞特异性NR3C1过表达小鼠和体外NR3C1增强β细胞的潜在保护作用,并发现EGCG通过抑制过度自噬来保护胰腺β细胞免受NR3C1增强诱导的衰竭。RNA去甲基化酶FTO(FTO α-酮戊二酸依赖双加氧酶)导致三个促氧化基因(Tlr4、Rela、Src)mRNA上的m6A修饰减少,因此发生氧化应激;相反,EGCG促进NR3C1增强的β细胞中泛素-蛋白酶体系统降解FTO,从而减轻氧化应激,防止过度自噬。此外,FTO过表达消除了EGCG对NR3C1增强诱导的β细胞损伤的作用。总之,该研究表明,EGCG通过抑制FTO刺激的氧化应激,保护胰腺β细胞免受NR3C1增强诱导的过度自噬,这为EGCG抗糖尿病作用的机制提供了新的见解。
六、国自然中标情况

 文章推荐
文章推荐